- Accueil
- volume 13 (2009)
- numéro 4
- La vaccination contre la maladie de Newcastle chez le poulet (Gallus gallus)
Visualisation(s): 89305 (409 ULiège)
Téléchargement(s): 2109 (11 ULiège)
La vaccination contre la maladie de Newcastle chez le poulet (Gallus gallus)

Notes de la rédaction
Reçu le 30 janvier 2009, accepté le 11 mai 2009
Résumé
La maladie de Newcastle (ND), dénommée également pseudo-peste aviaire, est une maladie hautement contagieuse et dévastatrice de la volaille. Elle est provoquée par certains paramyxovirus aviaires de sérotype 1, appelés virus de la maladie de Newcastle (NDV). Le NDV est capable d'infecter plus de 200 espèces d'oiseaux différentes mais la virulence de ce virus ainsi que les signes cliniques de la ND varient fortement selon l'espèce hôte et la souche virale. Tout isolement de souches vélogènes doit être notifié à l'Organisation Mondiale de la Santé Animale (OMSA, ex-OIE). L'objectif des différentes stratégies de prévention de la ND est de prévenir l'apparition ou de limiter les conséquences cliniques et économiques de la maladie, en évitant le contact par des mesures de biosécurité et/ou en renforçant la résistance à l'infection des oiseaux sensibles par la vaccination. A l'heure actuelle, les vaccins commerciaux les plus fréquemment utilisés sont des souches virales atténuées (vaccins « vivants ») de virulence nulle (souches apathogènes), faible (lentogènes) ou modérée (mésogènes). Des vaccins inertes sont également employés. Les programmes de vaccination varient néanmoins fortement d'un pays voire d'un élevage à l'autre. Classiquement, la bonne prise vaccinale est vérifiée par la réponse humorale des volailles. Cependant, le niveau de protection induit par la vaccination n'est pas toujours directement corrélé au taux d'anticorps circulants et dans les conditions de terrain, les programmes de vaccination actuels ne protègent pas, ou peu, contre l'excrétion de virus sauvage. En effet, l'efficacité vaccinale est fortement affectée par la présence chez les jeunes animaux d'anticorps maternels en quantité variable selon l'élevage, le lot de poussins et l'individu. Enfin, les souches vaccinales sont phylogénétiquement éloignées des souches virulentes circulantes. Ainsi, de nouveaux candidats vaccins, moins sensibles aux anticorps maternels et plus proches génétiquement des souches circulantes sont investigués en laboratoire afin d'améliorer l'efficacité des vaccins commerciaux conventionnels, tandis que de nouveaux outils de mesure de l'immunité sont développés pour une meilleure définition des mécanismes de protection induits par la vaccination.
Abstract
Vaccination against Newcastle disease in chickens. Newcastle Disease (ND), also fowl pest, is a highly contagious and devastating disease in poultry. It is induced by an avian paramyxoviruses serotype 1, named ND virus (NDV). NDV has been shown to be able to infect over 200 different species of birds but the virulence of this virus and clinical signs of ND vary largely with both host and strain of virus. Virulent strains require to be reported to the World Organisation for Animal Health (OIE) and outbreaks result in strict embargoes for the trade of avian products among countries. Control of ND primarily consists of vaccination of flocks and culling of infected or likely infected birds. At the present time, vaccination programs for NDV include the use of either inactivated (killed) or attenuated (live) vaccines to induce protective immunity while producing minimal adverse reactions in birds. Live viruses of low virulence (apathogenic, lentogenic) or of moderate virulence (mesogenic) are used depending on the disease situation and the regulations. Nevertheless, vaccination schedules might vary among poultry breeds. Generally, post-vaccination serology is used to confirm successful application of vaccine and an adequate immune response by the bird. However, it is well recognized that many chickens with low or no antibody titer are protected in challenge experiments and that present vaccination schedules do not protect well against viral re-excretion. One of the most important considerations affecting vaccination programs is the level of maternal immunity in young chickens, which may vary considerably from farm to farm and among individual chickens. Additionally, vaccine strains are phylogenetically different from circulating virulent strains. Then, new vaccines candidates are investigated in laboratory to improve the efficacy of conventional commercial vaccines while new tools of immunity measure are developed to increase the understanding of the protective immune response against NDV.
Table des matières
1. La maladie de Newcastle
1.1. Introduction
1La maladie de Newcastle (Newcastle Disease, ND), ou pseudo-peste aviaire, est une maladie virale hautement contagieuse qui peut affecter un grand nombre d'espèces aviaires et causer de sévères pertes économiques dans de nombreux pays. L'agent responsable est appelé virus de la maladie de Newcastle (Newcastle Disease Virus : NDV) ou paramyxovirus aviaire de type-I (Avian paramyxovirus type 1, APMV-I). Les premiers cas de ND ont été décrits en 1926 à Java, en Indonésie (Kraneveld, 1926) et à Newcastle-upon-Tyne, en Angleterre (Doyle, 1927).
2L'impact économique du NDV est énorme et ne doit pas uniquement être mesuré en termes de pertes commerciales directes (mortalités). Dans les pays développés indemnes de la maladie, les mesures de contrôle, telles que la vaccination, et les tests répétés afin de maintenir leur statut indemne représentent une perte énorme pour l'industrie avicole. Dans les pays en voie de développement où les œufs et la viande de volaille constituent la principale source de protéines alimentaires, le NDV, de par sa circulation endémique, représente un frein au développement de la production avicole.
3En termes de santé publique, parallèlement à sa contribution à la malnutrition, la ND est considérée comme une anthropozoonose mineure. La transmission à l'homme est anecdotique et se traduit par une infection oculaire, telle qu'une conjonctivite, des paupières oedémateuses et des larmoiements. Des maux de tête et de la fièvre sont parfois observés, accompagnés ou non de conjonctivite (Capua et al., 2004).
1.2. L'agent pathogène
4Le NDV est un virus enveloppé qui fait partie du genre récemment décrit des Avulavirus appartenant à la famille des Paramyxoviridae (Alexander, 2003). Cette famille de virus se caractérise par une capside de symétrie hélicoïdale et par un ARN monocaténaire non segmenté de polarité négative. Neuf sérotypes ont été identifiés au sein des paramyxovirus aviaires (APMV-1 à APMV-9), le NDV appartenant au sérotype 1. Ce virus présente de grandes diversités génétiques, ces dernières étant associées à l'origine spatio-temporelle ainsi qu'à l'espèce hôte des différentes souches. Ainsi, le séquençage du gène de la protéine de fusion F a permis d'identifier au moins six lignées distinctes de NDV (lignées 1 à 6) (Aldous et al., 2003), tandis que l'analyse génétique complète du génome a révélé l'existence de deux divisions majeures, à savoir les classes I et II, la seconde classe pouvant être subdivisée en huit génotypes (génotype I à VIII) (Tableau 1) (Czegledi et al., 2006). Bien que toutes les souches de NDV appartiennent au même sérotype (APMV-1), ces variations génétiques pourraient avoir un impact sur l'antigénicité et donc sur l'efficacité des campagnes de vaccination (Miller et al., 2007) (voir plus loin dans le texte).
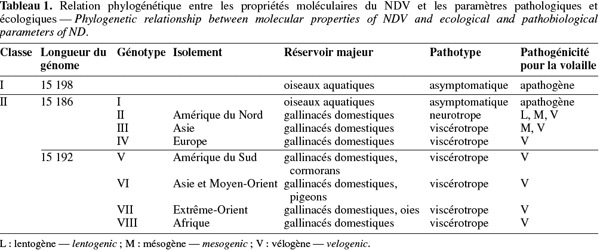
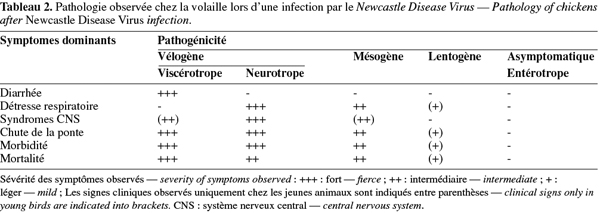
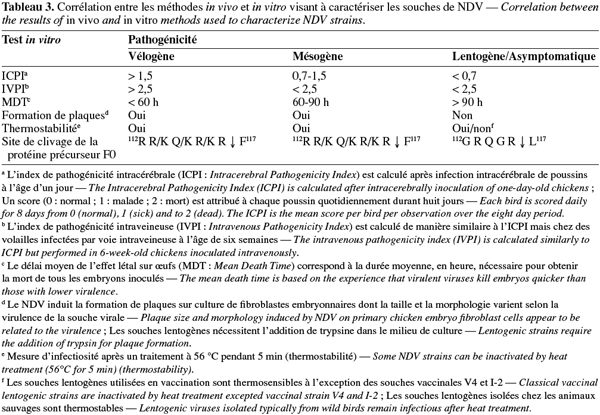
5La virulence des souches de NDV varie fortement selon l'espèce aviaire hôte. Les canards et les oies (Ansériformes) peuvent être infectés mais ne montrent que peu ou pas de signes cliniques, tandis que les poules et les dindes (Galliformes) sont hautement sensibles. Les pigeons peuvent également être infectés par des paramyxovirus de pigeons, ceux-ci pouvant par la suite s'adapter aux volailles. Les oiseaux sauvages sont quant à eux considérés comme des hôtes réservoirs. Chez les poules, le pouvoir pathogène du NDV diffère cependant d'une souche virale à l'autre. Ainsi, les souches virales ont été classées en cinq pathotypes sur base des signes cliniques observés chez les volailles infectées expérimentalement (Tableau 2) (Alexander, 2003). D'autres tests sont également utilisés pour établir la virulence des différentes souches du NDV (Tableau 3). L'index de pathogénicité intracérébrale (ICPI, Intracerebral Pathogenicity Index) chez le poussin d'un jour est le test officiel de mesure de virulence. En effet, selon la directive européenne 92/66/EEC, les souches de NDV possédant un ICPI moyen supérieur à 0,7 sont considérées comme virulentes. En accord avec la nouvelle définition des maladies épizootiques notifiables, tout isolement de ces souches doit être rapporté à l'Organisation Mondiale de la Santé Animale (OMSA, ex-OIE, Office International des Epizooties). Plus récemment, les techniques de biologie moléculaire, telles que la PCR et le séquençage, ont permis d'identifier les bases moléculaires de la pathogénicité du NDV, à savoir la présence d'acides aminés basiques supplémentaires au niveau du site de clivage de la glycoprotéine précurseur F0 en F1 et F2 chez les souches vélogènes et mésogènes (Peeters et al., 1999 ; Römer-Oberdörfer et al., 2003 ; 2006 ; De Leeuw et al., 2005 ; Wakamatsu et al., 2006) ainsi que la longueur et la conformation de la protéine haemagglutinine neuraminidase HN (Römer-Oberdörfer et al., 2003 ; 2006 ; Huang et al., 2004 ; De Leeuw et al., 2005). Le séquençage du site de clivage du gène F est actuellement accepté comme test alternatif à l'ICPI par les instances officielles (Union européenne, OIE).
1.3. Pathologie et épidémiologie
6Incidence et distribution. La ND est enzootique à travers la majorité de l'Afrique, le Moyen-Orient, l'Asie, l'Amérique Centrale et la partie nord de l'Amérique du Sud. Dans les zones plus développées, telles que l'Europe de l'Ouest et les USA, des épizooties sporadiques sont encore observées, malgré la large utilisation de vaccins.
7Les études épidémiologiques ont indiqué que plusieurs épizooties de ND ont eu lieu depuis les premiers cas décrits de la maladie (Yu et al., 2001 ; Czegledi et al., 2006). Premièrement, les génotypes II, III et IV ont été enzootiques en Amérique du Nord, en Asie et en Europe, respectivement, durant les années 1930 et 1940. Les souches NDV de génotypes VI ont ensuite émergé en épizooties au Moyen-Orient et en Asie durant les années 1960, tandis que celles du génotype V se sont manifestées en Amérique du Nord et en Europe au début des années 1970. La quatrième épizootie a eu lieu durant les années 1990 au Moyen-Orient suite à la prévalence du génotype VII. Le génotype VIII a été endémique en Afrique du Sud durant la décennie précédente. Comme le montre le tableau 1, les souches NDV circulant actuellement à travers le monde sont essentiellement viscérotropes.
8Signes cliniques, morbidité et mortalité. Lors d'une exposition naturelle, la période d'incubation du NDV varie de 2 à 15 jours. Généralement, les signes cliniques de la ND sont une dépression, une diarrhée, un état de prostration, des oedèmes autour des yeux ainsi qu'un(e) diminution/arrêt de la ponte. La mortalité et les signes nerveux (torticolis, clonies, etc.) sont très souvent présents. Les lésions hémorragiques du proventricule et de l'intestin sont quasi constantes. Cependant, certaines différences peuvent être faites selon le pathotype de la maladie, telles que décrites précédemment (Tableau 2).
9Transmission. La transmission du NDV entre volailles a lieu par voie oro-fécale. Suite à la multiplication du NDV dans leur tractus respiratoire et/ou digestif, les volailles infectées excrètent le virus par voie aérogène et/ou fécale. Des gouttelettes et des aérosols contaminés peuvent ensuite être inhalés par les volailles saines ou affecter leurs muqueuses, tandis que les matières fécales risquent de contaminer la nourriture et l'eau de boisson et être ainsi ingérées par les autres oiseaux du poulailler.
10La dispersion du virus peut également se faire d'un élevage à l'autre via le transport de matériel contaminé (sol, litière, équipement). En effet, bien qu'il s'agisse d'un virus enveloppé, le NDV est relativement stable à l'extérieur de l'hôte et peut survivre plusieurs jours, voire plusieurs mois, en présence de matières organiques, selon la température et l'humidité environnante. Ce mode de transmission explique pourquoi un épisode de ND peut rapidement évoluer en épizootie. A l'heure actuelle, la possibilité d'une transmission verticale est controversée (Capua et al., 1993 ; Chen et al., 2002 ; Roy et al., 2005).
2. La vaccination du poulet contre la maladie de Newcastle
2.1. Les stratégies de prévention et de contrôle de la ND
11L'objectif des différentes stratégies de prévention est, d'une part, d'empêcher l'infection des oiseaux sensibles et, d'autre part, de réduire le nombre d'oiseaux sensibles par la vaccination. La biosécurité et l'hygiène sont considérées comme les premières lignes de protection contre l'introduction de toute maladie aviaire et en particulier contre la ND (Bermudez, 2003 ; Bermudez et al., 2003). Ainsi, les mouvements de personnes (éleveurs, vétérinaires, livreurs, etc.) et de véhicules doivent être limités et accompagnés de désinfections et du changement de vêtements et de chaussures et ce, y compris en l'absence de maladie. Il convient également de prévenir le contact direct et indirect des volailles avec les oiseaux sauvages ou les pigeons. En raison des couts qu'elles engendrent, les mesures de filtration d'air et de surpression visant à limiter l'entrée aérienne de virions dans le poulailler sont essentiellement réservées aux élevages de haute valeur génétique et aux parentales.
12Quoique la biosécurité puisse s'avérer suffisante, la vaccination est considérée comme une précaution supplémentaire, en particulier dans les zones à haute densité de populations de volailles (Densely Populated Poultry Area, DPPA). Ainsi, la vaccination préventive fait également partie des mesures prophylactiques globales contre la ND. En effet, la vaccination de masse pratiquée en aviculture vise à limiter le risque d'infection des volailles par le NDV et à réduire la transmission virale, tout en prévenant les signes cliniques et la mortalité. La politique de vaccination varie cependant selon le statut endémique et la perspective d'émergence de la ND ou selon la situation géographique. Ainsi, dans les pays où le NDV est absent et constitue une menace épizootique, le but de la vaccination est d'assurer une protection maximale contre la ND. C'est notamment le cas au niveau européen avec la Belgique, les Pays-Bas et l'Allemagne où la vaccination a été rendue obligatoire sur tous les types de production depuis les années 1990 suite aux épidémies de ND. Dans d'autres pays comme la France, ne sont vaccinées que les volailles à vie longue (pondeuses et reproductrices). Dans les pays où le NDV est enzootique, la vaccination visera une diminution de la pression d'infection. La maladie peut dès lors ne pas se manifester en raison de la campagne de vaccination menée. Enfin, des pays comme la Suède, la Finlande et l'Estonie ne vaccinent pas du tout et refusent dès lors toute forme d'introduction du NDV sur leur territoire. L'Europe autorise uniquement l'utilisation de certains vaccins atténués spécifiques et considère d'autres vaccins comme étant d'une virulence non acceptable (souches mésogènes).
13Enfin, les mesures prises pour éradiquer la ND lors d'une épizootie sont déterminées en fonction de divers facteurs tels que le nombre, le type et la densité d'élevages aviaires de la région, du pays. Ainsi, dans les zones à plus faible densité, une politique d'éradication est adoptée avec abattage des oiseaux infectés, des oiseaux en contact ainsi que de leurs produits suivi du nettoyage et de la désinfection du poulailler (assainissement). Une telle politique inclut généralement des restrictions d'échanges et de commerce d'oiseaux dans une zone de quarantaine définie autour du foyer pendant au moins 21 jours à partir du dernier foyer. Ces mêmes mesures d'assainissement sont prises dans les pays à forte densité avicole, accompagnées ou non d'une vaccination d'urgence des oiseaux dans une zone tampon autour du foyer infectieux (« vaccination en anneau »).
2.2. Les principaux types de vaccins
14Les deux types de vaccins contre la ND commercialisés aujourd'hui sont les vaccins à virus atténués et les vaccins à virus inactivés (encore improprement appelés « vaccins tués ») dont les caractéristiques générales sont reprises dans le tableau 4 (Bermudez et al., 2003 ; Marangon et al., 2006).
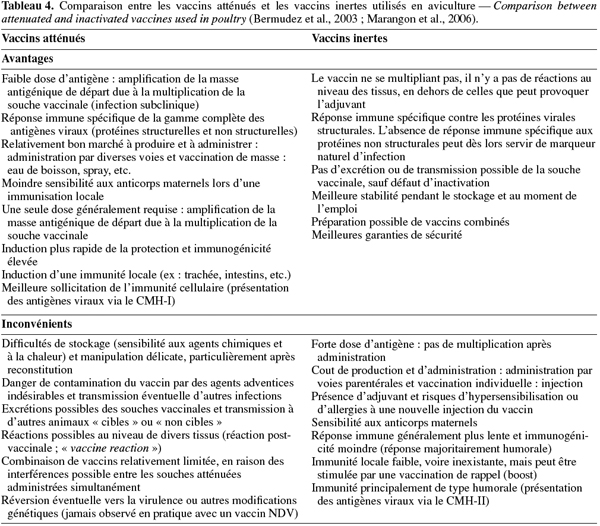
15Les souches de NDV utilisées en tant que vaccins atténués se divisent en deux groupes, à savoir les souches lentogènes et les souches mésogènes (European Food Safety Authority, 2007). Seules les souches lentogènes sont autorisées en Europe et doivent répondre à la Directive européenne 93/152/EEC. Sont utilisées les souches Hitchner B1, La Sota, Clone 30, Ulster 2C, VG/GA, Phy LMV42, C131, Brescia et C2, selon différentes dénominations commerciales. D'autres souches lentogènes sont également utilisées en dehors des frontières européennes, à savoir les souches V4 Queensland, I-2 et F. Des vaccins à base de souches mésogènes, telles que Mukteswar, Komarov et Roakin, sont utilisés dans les pays où la ND est endémique, au Moyen-Orient, en Afrique et en Asie essentiellement, alors qu'ils sont interdits dans l'Union européenne (Directive européenne 93/152/EEC).
16Les souches vaccinales pré-citées peuvent également être inactivées par différents procédés physiques (chaleur, rayons UV) ou chimiques (traitement au formol, à l'éthylèneimine binaire ou à la β-propiolactone) pour la production de vaccins inertes. Ces vaccins sont combinés avec des adjuvants huileux pour former une émulsion et sont classiquement utilisés en vaccination de rappel chez les poules pondeuses et reproductrices, en combinaison avec d'autres valences (maladie de Gumboro, bronchite infectieuse) avant l'entrée en ponte.
2.3. Les voies d'inoculation
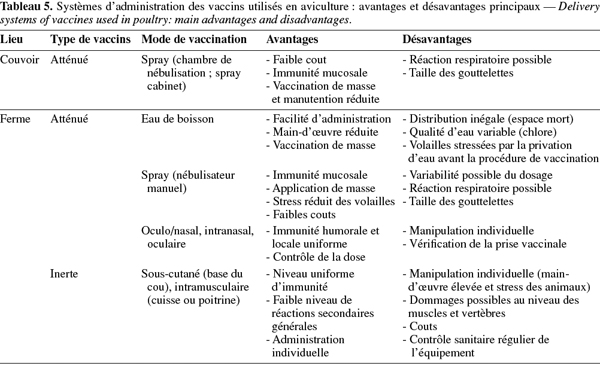
17Le système d'administration des vaccins influence le niveau de protection obtenu. L'application incorrecte du vaccin est considérée comme une des raisons les plus communes d'échec de campagne de vaccination. Le choix de la méthode de vaccination dépend du lieu (couvoir ou ferme), du type de production, de l'espèce aviaire, de la taille du poulailler, de la longueur du cycle de production, du statut sanitaire général, de l'immunité maternelle, des vaccins à appliquer et des couts. Ainsi, les vaccins atténués contre la ND peuvent être administrés, soit par voie oculaire (gouttes dans l'œil), intra-nasale (goutte dans le nez) ou oculo/nasale (technique de trempage du bec) pour une application individuelle, soit par voie orale (eau de boisson ou nourriture) ou oculo/nasale et respiratoire (spray, nébulisation) lors d'une application de masse. L'application individuelle de vaccins atténués reste restreinte aux petits élevages et en cas de risques sévères d'infection, en raison du travail supplémentaire qu'elle engendre. Les vaccins inertes ne peuvent quant à eux être utilisés qu'individuellement par injection, soit intramusculaire, soit sous-cutanée. Les principaux avantages et inconvénients de ces vaccins sont repris dans le tableau 5 (Marangon et al., 2006).
2.4. Les principaux programmes de vaccination
18Dans les élevages industriels, la vaccination aviaire contre le ND est une vaccination de masse qui vise à limiter l'infection des volailles et à réduire la transmission virale, tout en prévenant les signes cliniques et la mortalité. En outre, la réussite vaccinale est fortement affectée par le niveau d'anticorps maternels (Maternally-Derived Antibody, MDA) des jeunes volailles, celui-ci pouvant varier fortement selon l'élevage, le lot de poussins et l'individu. D'autre part, les programmes de vaccination contre la ND varient selon le type d'élevage (poules pondeuses, reproductrices, poulets de chair). Enfin, les vaccins atténués les plus immunogènes sont également ceux qui possèdent la pathogénicité résiduelle la plus élevée et peuvent de ce fait provoquer davantage d'effets adverses, notamment chez les jeunes animaux. Il convient dès lors d'utiliser en primo-vaccination une souche lentogène très atténuée (Hitchner B1, Ulster 2C, Phy-LMV 42) suivie d'une souche plus virulente (La Sota) à quelques semaines d'intervalle. Plusieurs stratégies vaccinales peuvent dès lors être envisagées et la durée de l'immunité induite dépend du programme de vaccination choisi. Dans les conditions de l'Europe de l'Ouest, les poules pondeuses et les reproductrices sont généralement vaccinées une première fois à l'aide de vaccins atténués entre l'âge de 2 et 4 semaines (après la chute des MDA) puis font l'objet de rappels de vaccination, à intervalles variables, avec des vaccins moins atténués. Une injection de vaccin inerte est enfin réalisée avant la période de reproduction, afin de protéger l'animal en ponte et, dans le cas de reproductrices, pour maintenir une immunité maternelle optimale chez leur progéniture. Les poulets de chair, ayant une durée de vie plus courte, sont très généralement vaccinés à l'âge d'un jour à l'aide de vaccins atténués, permettant d'établir une infection active qui peut persister chez certains au-delà de l'immunité maternelle. En raison de cette interférence des MDA, une deuxième vaccination à l'âge de 2-3 semaines est nécessaire et obligatoire pour assurer une bonne protection du troupeau.
2.5. Le suivi de la réponse immune induite par la vaccination
19Classiquement, la réponse immune induite par la vaccination contre la ND est évaluée par le titre en anticorps inhibant l'haemagglutination (Haemagglutination Inhibition, HI). Ce titre dépend notamment du vaccin utilisé et de sa voie d'inoculation, du programme de vaccination suivi ainsi que de facteurs environnementaux et individuels. Ainsi, un titre HI entre 24 et 26 peut être obtenu suite à une unique inoculation d'un vaccin atténué, tandis qu'un titre avec un pic supérieur à 211 ne peut être atteint que suite à un programme de vaccination incluant un vaccin inactivé. Cependant, chez des animaux vaccinés, la protection contre la mortalité, les signes cliniques et/ou l'excrétion de virus sauvage lors d'une épreuve virulente létale sans anticorps détectables en HI ont été décrits (Gough et al., 1973). Ceci peut s'expliquer par une immunité locale et/ou par une réponse immune de type cellulaire.
2.6. Les limites des programmes de vaccination actuels
20Comme énoncé au cours des chapitres précédents, l'approche classiquement utilisée pour la vaccination aviaire contre la ND comporte certains inconvénients et limites, parmi lesquels l'interférence des MDA, une protection face à une épreuve très virulente qui peut varier de 25 à 80 % selon les conditions de terrain, des réactions secondaires à la vaccination avec comme conséquences des effets négatifs sur les performances zootechniques (retards de croissance et baisses de conversion alimentaire). De plus, les souches virulentes circulant à travers le monde depuis les années 1970 sont de génotype V-VIII, tandis que les souches vaccinales utilisées en Europe appartiennent aux génotypes I et II. Cette divergence explique qu'une souche vaccinale éloignée au niveau phylogénétique des souches circulantes n'assure pas une protection aussi optimale, en termes d'excrétion de virus sauvage, qu'une souche vaccinale homologue (Miller et al., 2007).
2.7. Les nouvelles stratégies vaccinales
21Comme indiqué antérieurement, les vaccins actuellement commercialisés peuvent manquer d'efficacité et présenter certains inconvénients d'utilisation. La mise en œuvre des techniques de biologie moléculaire dans le domaine de la vaccination a pour objectifs une amélioration, d'une part, de l'efficacité et d'autre part, de l'innocuité des vaccins conventionnels. Les recherches peuvent aussi s'orienter vers la mise au point de nouveaux types de vaccins, soit vectorisés, soit sous-unitaires (développés à partir des seuls éléments immunogènes du virus, principalement les protéines de surface ou de l'enveloppe virale). Enfin, de nouveaux adjuvants sont envisagés.
22Ainsi, l'inconvénient majeur des vaccins atténués est leur pathogénicité résiduelle et leurs effets adverses, notamment chez les jeunes animaux. Des vaccins vectorisés contenant un ou plusieurs gènes du NDV ont dès lors été étudiés comme alternative, à savoir les vecteurs poxvirus aviaire (Fowl Poxvirus, FPV) (Boursnell et al., 1990 ; Taylor et al., 1990 ; Iritani et al., 1991 ; Nagy et al., 1991 ; McNillen et al., 1994 ; Karaca et al., 1998) et le virus herpès de la dinde (Herpesvirus of Turkey, HVT) (Morgan et al., 1992 ; 1993 ; Heckert et al., 1996 ; Reddy et al., 1996). Ce type de vaccin présente l'avantage d'être bivalent, puisqu'il induit une immunité contre la maladie spécifique du gène inséré dans le vecteur, mais également une immunité spécifique de la variole aviaire et de la maladie de Marek, dans le cas du vecteur fowlpox et HVT, respectivement. En outre, ces vaccins vectorisés rendent possible l'adaptation de l'insert en fonction des souches de NDV circulantes. Actuellement, seuls deux vaccins fowlpox recombinants NDV sont commercialisés : le Vectormune FP-ND (Ceva Biomune), vaccin lyophilisé et le Trovac-NDV (Merial), produit conservé en azote liquide. Ces vaccins fowlpox recombinants sont injectés en sous-cutanée, ou selon la technique de transfixion alaire au niveau de la palmure de l'aile (technique dite wing web) et nécessitent donc une manipulation individuelle des animaux à inoculer. Leur second désavantage éventuel est leur sensibilité aux MDA dirigés contre le vecteur lui-même (Iritani et al., 1991 ; Swayne et al., 2000) et dès lors la difficulté d'utiliser de tels vecteurs chez les animaux vaccinés contre la variole aviaire. Les vecteurs herpesvirus sont quant à eux nettement moins sensibles à cette interférence (Morgan et al., 1993) et présentent également l'avantage majeur de pouvoir être administrés in ovo (Reddy et al., 1996 ; Johnston et al., 1997). A l'heure actuelle, deux vaccins de type HVT recombinants NDV sont commercialisés : le Vectormune HVT-ND (Ceva Biomune) et l'Innovax ND (Shering Plough Intervet).
23La vaccination in ovo constitue une alternative avantageuse à la vaccination de masse car elle permet de vacciner les volailles avant leur naissance. En effet, cette technologie présente l'avantage d'être réalisée sur des œufs embryonnés d'environ 18 jours, c'est-à-dire au moment où les œufs sont transférés des incubateurs vers les éclosoirs et avant la résorption des MDA. Elle permet dès lors d'éviter une manipulation des volailles durant leur période de croissance et l'interférence des MDA. Cependant, les souches vaccinales NDV usuelles tuent ou affaiblissent l'embryon et réduisent dès lors fortement le pourcentage d'éclosion. Des souches à pathogénicité davantage réduite pour l'embryon ont été sélectionnées pour leur utilisation in ovo (Mast et al., 2006). Ces vaccins se sont avérés efficaces à petite échelle, y compris en présence de MDA.
24D'autres essais, tels que l'immunisation à l'aide de complexes immuns NDV sous forme d'émulsion huileuse (Pokric et al., 1993) ou de plasmides dans lesquels sont clonés les gènes des protéines F et/ou HN (Sakaguchi et al., 1996 ; Loke et al., 2005) ont été testés en laboratoire mais ne sont pas développés à l'échelle industrielle. Enfin, le NDV est actuellement évalué en tant que support d'expression d'antigènes étrangers tels que le gène de l'hémagglutinine du virus de l'Influenza aviaire (Swayne et al., 2003 ; Veits et al., 2006). Ce type de vaccin recombinant permettrait ainsi la vaccination conjointe contre la maladie de Newcastle et contre la grippe aviaire.
25D'autres stratégies vaccinales ont été investiguées en laboratoire afin de pallier le cout de production élevé des vaccins inertes, telles que l'injection sous-cutanée de la protéine HN du NDV produite in vitro par un baculovirus recombinant (Nagy et al., 1991). Cependant, ce type de vaccin sous-unitaire n'est pas encore commercialisé à l'heure actuelle en raison de son cout de production et du droit d'utilisation des systèmes recombinants.
26Enfin, différents types d'adjuvants, tels que la toxine du choléra (Takada et al., 1996), des séquences immunostimulatrices d'ADN (Linghua et al., 2007 ; Zhang et al., 2008) et les cytokines aviaires (Marcus et al., 1999 ; Degen et al., 2005 ; Yin et al., 2007) ont été étudiés chez la volaille afin d'améliorer et/ou moduler la réponse immune locale au niveau des muqueuses et la réponse immune systémique induites à l'encontre d'antigènes du NDV administrés par voie locale. Leur efficacité reste cependant variable.
3. Conclusion
27En conclusion, bien que sa nécessité ait été démontrée et qu'elle soit obligatoire, les éleveurs sont souvent réticents à la vaccination contre la ND en raison de la charge de travail supplémentaire qu'elle représente et de son effet potentiellement négatif sur les performances de production. De plus, la vaccination selon les programmes actuels n'empêche ni l'infection des volailles vaccinées, ni l'excrétion de virus sauvage. Dans un contexte d'éradication de la ND, il est dès lors nécessaire de développer un « vaccin idéal » capable de protéger les animaux de la maladie et d'inhiber la dispersion du virus lors d'une infection, tout en limitant la charge de travail pour les éleveurs. Un vaccin inoculable in ovo et peu sensible aux MDA aurait dès lors un avantage déterminant.
28Par ailleurs, la sérologie n'expliquant pas à elle seule le niveau de protection induit par la vaccination, des recherches sont actuellement effectuées en laboratoire afin de mesurer de manière plus approfondie l'immunité à médiation cellulaire et la réponse immune locale (au niveau du tractus respiratoire et digestif) spécifique au NDV et leur rôle dans la protection contre les signes cliniques et l'excrétion du virus. Ces nouvelles techniques apporteront une meilleure connaissance des mécanismes de l'immunité induite par la vaccination et dès lors, des outils pour la sélection du « vaccin idéal » contre la ND.
Bibliographie
Aldous E.W., Mynn K.K., Banks J. & Alexander D.J., 2003. A molecular epidemiological study of avian paramyxovirus type 1 (Newcastle disease virus) isolates by phylogenetic analysis of a partial nucleotide sequence of the fusion protein gene. Avian Pathol., 32, 239-256.
Alexander D.J., 2003. Newcastle disease, other avian paramyxoviruses, and pneumovirus infections. In: Saif Y.M., ed. Diseases of poultry. Ames, IA, USA: Iowas State University Press, 63-87.
Bermudez A.J., 2003. Principles of disease prevention: diagnosis and control. In: Saif Y.M., ed. Diseases of poultry. Ames, IA, USA: Iowas State University Press, 3-60.
Bermudez A.J. & Stewart-Brown B., 2003. Disease prevention and diagnostic. In: Saif Y.M., ed. Disease of poultry. Ames, IA, USA: Iowas State University Press, 17-55.
Boursnell M.E.G. et al., 1990. A recombinant fowlpox virus expressing the hemagglutinin-neuraminidase gene of Newcastle disease virus (NDV) protects chickens against challenge by NDV. Virology, 178, 297-300.
Capua I., Scacchia M., Toscani T. & Caporale V., 1993. Unexpected isolation of virulent Newcastle disease virus from commercial embryonated fowls' eggs. J. Vet. Med. B, 40, 609-612.
Capua I. & Alexander D., 2004. Human health implications of avian influenza viruses and paramyxoviruses. Eur. J. Clin. Microbiol. Infect. Dis., 23, 1-6.
Chen J.P. & Wang C.H., 2002. Clinical epidemiologic and experimental evidence for the transmission of Newcastle disease virus through eggs. Avian Dis., 46, 461-465.
Czegledi A. et al., 2006. Third genome size category of avian paramyxovirus serotype 1 (Newcastle disease virus) and evolutionary implications. Virus Res., 120, 36-48.
De Leeuw O.S. et al., 2005. Virulence of Newcastle disease virus is determined by the cleavage site of the fusion protein and by both the stem region and globular head of the haemagglutinin-neuraminidase protein. J. Gen. Virol., 86, 1759-1769.
Degen W.G.J. et al., 2005. Potentiation of humoral immune responses to vaccine antigens by recombinant chicken IL-18 (rChIL-18). Vaccine, 23, 4212-4218.
Doyle T.M., 1927. A hitherto unrecorded disease of fowls due to a filter-passing virus. J. Comp. Pathol. Ther., 40, 144-169.
European Food Safety Authority (E.F.S.A.), 2007. Opinion of the scientific panel on animal health and animal welfare regarding a request from the European commission to review Newcastle disease focussing on vaccination worldwide to determine its optimal use for disease control purpose. E.F.S.A J., 477, 1-25.
Gough R.E. & Alexander D.J., 1973. The speed of resistance to challenge induced in chickens vaccinated by different routes with a B1 strain of live NDV. Vet. Rec., 92, 563-564.
Heckert R.A. et al., 1996. Onset of protective immunity in chicks after vaccination with a recombinant herpesvirus of turkeys vaccine expressing Newcastle disease virus fusion and hemagglutinin-neuraminidase antigens. Avian Dis., 40, 770-777.
Huang Z. et al., 2004. The hemagglutinin-meuraminidase protein of Newcastle disease virus determines tropism and virulence. J. Virol., 78, 4176-4184.
Iritani Y. et al., 1991. Antibody response to Newcastle disease virus (NDV) of recombinant fowlpox virus (FPV) expressing a hemagglutinin-neuraminidase of NDV into chickens in the presence of antibody to NDV or FPV. Avian Dis., 35, 659.
Johnston P.A. et al., 1997. Applications in in ovo technology. Poultr. Sci., 76, 165-178.
Karaca K. et al., 1998. Recombinant fowlpox viruses coexpressing chicken type I IFN and Newcastle disease virus HN and F genes: influence of IFN on protective efficacy and humoral responses of chickens following in ovo or post-hatch administration of recombinant viruses. Vaccine, 16, 1496-1503.
Kraneveld F.C., 1926. A poultry disease in the Dutch East Indies. Ned. Indisch Bl. Diergeneeskd, 38, 448-450.
Linghua Z., Xingshan T. & Fengzhen Z., 2007. Vaccination with Newcastle disease vaccine and CpG oligodeoxynucleotides induces specific immunity and protection against Newcastle disease virus in SPF chicken. Vet. Immunol. Immunopathol., 115, 216-222.
Loke C.F., Omar A.R., Raha A.R. & Yusoff K., 2005. Improved protection from velogenic Newcastle disease virus challenge following multiple immunizations with plasmid DNA encoding for F and HN genes. Vet. Immunol. Immunopathol., 106, 259-267.
Marangon S. & Busani L., 2006. The use of vaccination in poultry production. Rev. Sci. Techn. Off. Int. Epizoot., 26, 265-274.
Marcus P.I., van der Heide L. & Sekellick M.J., 1999. Interferon action on avian viruses. I. Oral administration of chicken interferon-alpha ameliorates Newcastle disease. J. Interferon Cytokine Res., 19, 881-885.
Mast J. et al., 2006. Vaccination of chickens embryos with escape mutants of La Sota Newcastle disease virus induces a protective immune response. Vaccine, 24, 1756-1765.
McNillen J.K. et al., 1994. The safe and effective use of fowlpox virus as vector for poultry vaccines. Dev. Specif. Biotechnol. Pharm. Prod., 82, 137-145.
Miller P.J., King D.J., Afonso C.L. & Suarez D.L., 2007. Antigenic differences among Newcastle disease virus strains of different genotypes used in vaccine formulation affect viral shedding after a virulent challenge. Vaccine, 27, 7238-7246.
Morgan R.W. et al., 1992. Protection of chickens from Newcastle and Marek'diseases with a recombinant herpesvirus of turkeys vaccine expressing the Newcastle disease virus fusion protein. Avian Dis., 36, 858-870.
Morgan R.W., Gelb J.J., Pope C.R. & Sondermeijer P.J.A., 1993. Efficacy in chickens of a herpesvirus of turkeys recombinant vaccine containing the fusion gene of Newcastle disease virus: onset of protection and effect of maternal antibodies. Avian Dis., 37, 1032-1040.
Nagy E., Krell P.J., Dulac G.C. & Derbyshire J.B., 1991. Vaccination against Newcastle disease with a recombinant baculovirus hemagglutinin-neuraminidase subunit vaccine. Avian Dis., 35, 585-590.
Peeters B.P.H., de Leeuw O.S., Koch G. & Gielkens A.L.J., 1999. Rescue of Newcastle disease virus from cloned cDNA: evidence that cleavability of the fusion protein is a major determinant for virulence. J. Virol., 73, 5001-5009.
Pokric B., Sladic D., Juros S. & Cajavec S., 1993. Application of the immune complex for immune protection against viral disease. Vaccine, 11, 655-659.
Reddy S.K. et al., 1996. Protective efficacy of a recombinant herpesvirus of turkeys as an in ovo vaccine against Newcastle and Marek's diseases in specific-pathogen-free chickens. Vaccine, 14, 469-477.
Römer-Oberdörfer et al., 2003. Contribution of the length of the HN protein and the sequence of the F protein cleavage site to Newcastle disease virus pathogenicity. J. Gen. Virol., 84, 3121-3129.
Römer-Oberdörfer A., Veits J., Werner O. & Mettenleiter T.C., 2006. Enhancement of pathogenicity of Newcastle disease virus by alteration of specific amino acid residues in the surface glycoprotein F and HN. Avian Dis., 50, 259-263.
Roy P. & Venugopalan A.T., 2005. Unexpected Newcastle disease virus in day old commercial chicks and breeder hen. Comp. Immunol. Microbiol. Infectious Dis., 28, 277-285.
Sakaguchi M. et al., 1996. Protection of chickens from Newcastle disease by vaccination with a linear plasmid DNA expressing the F protein of Newcastle disease virus. Vaccine, 14, 747-752.
Swayne D.E. et al., 2000. Protection against diverse highly pathogenic H5 avian influenza viruses in chickens immunized with a recombinant fowlpox vaccine containing an H5 avian influenza hemagglutinin gene insert. Vaccine, 18, 1088-1095.
Swayne D.E. et al., 2003. Recombinant paramyrovirus type 1-avian influenza-H7 virus as a vaccine for protection of chickens against influenza and Newcastle disease. Avian Dis., 47, 1047-1050.
Takada A. & Kida H., 1996. Protective immune response of chickens against Newcastle disease, induced by the intranasal vaccination with inactivated virus. Vet. Microbiol., 50, 17-25.
Taylor J. et al., 1990. Newcastle disease virus fusion protein expressed in a fowlpox virus recombinant confers protection in chickens. J. Virol., 64, 1441-1450.
Veits J. et al., 2006. Newcastle disease virus expressing H5 hemagglutinin gene products chickens against Newcastle disease and avian influenza. Proc. Nat. Acad. Sci. USA, 103, 8197-8202.
Wakamatsu N. et al., 2006. The effect on pathogenesis of Newcastle disease virus La Sota strain from a mutation of the fusion cleavage site to a virulente sequence. Avian Dis., 50, 483-488.
Yin J. et al., 2007. Synergistic effects of adjuvants interferon-g and levamisole on DNA vaccination against infection with Newcastle disease virus. Viral Immunol., 20, 288-299.
Yu L. et al., 2001. Characterization of newly emerging Newcastle disease virus isolates from the people's republic of China and Taiwan. J. Clin. Microbiol., 39, 3512-3519.
Zhang L. et al., 2008. Enhancement of mucosal immune responses by intranasal co-delivery of Newcastle disease vaccine plus CpG oligonucleotide in SPF chickens in vivo. Res. Vet. Sci., 85, 495-502.
Pour citer cet article
A propos de : Fabienne Rauw
Centre d'Etudes et de Recherches Vétérinaires et Agrochimiques (CERVA). Département de Virologie et d'Immunologie. Rue Groeselenberg, 99. B-1180 Bruxelles (Belgique). E-mail : farau@var.fgov.be
A propos de : Yannick Gardin
CEVA Santé Animale. Direction scientifique. BP 126. F-33501 Libourne (France).
A propos de : Thierry van den Berg
Centre d'Etudes et de Recherches Vétérinaires et Agrochimiques (CERVA). Département de Virologie et d'Immunologie. Rue Groeselenberg, 99. B-1180 Bruxelles (Belgique).
A propos de : Bénédicte Lambrecht
Centre d'Etudes et de Recherches Vétérinaires et Agrochimiques (CERVA). Département de Virologie et d'Immunologie. Rue Groeselenberg, 99. B-1180 Bruxelles (Belgique).






