- Accueil
- Volume 29 (2025)
- Numéro 2
- Structure et stock de carbone des différents types de végétation de la réserve écologique de Borotou-Koro au Centre-Ouest de la Côte d’Ivoire
Visualisation(s): 811 (25 ULiège)
Téléchargement(s): 185 (15 ULiège)
Structure et stock de carbone des différents types de végétation de la réserve écologique de Borotou-Koro au Centre-Ouest de la Côte d’Ivoire

Document(s) associé(s)
Version PDF originaleRésumé
Description du sujet. Les écosystèmes forestiers jouent un rôle important dans l’atténuation du changement climatique à travers la réduction du dioxyde de carbone qui est un gaz à effet de serre.
Objectifs. Décrire le profil structural et estimer les stocks de carbone dans les différents types de végétation de la réserve écologique de Borotou-Koro en Côte d’Ivoire.
Méthode. Les données ont été collectées dans 30 parcelles de 2 500 m² (50 m x 50 m), délimitées sur trois types de végétation (forêt ripicole, forêt claire et savane) de la réserve écologique. Les mesures dendrométriques, effectuées sur tous les arbres de dbh ≥ 5 cm et portant sur le diamètre et la hauteur, ont permis de déterminer le profil structural, d’estimer la biomasse et le stock de carbone correspondant, en utilisant des équations allométriques de chaque biotope.
Résultats. La forêt claire possède les plus fortes valeurs de densité de peuplement (254 ± 60,44 tiges·ha-1) et de surface terrière (31,51 ± 10,57 m²·ha-1). La répartition par classe de diamètre des arbres dans les trois milieux présente l’allure d’un « J » renversé et s’ajuste au mieux avec des fonctions polynômes. La réserve écologique séquestre une quantité de carbone non négligeable estimée à 67,03 ± 12,89 t·ha-1. La forêt claire stocke plus de carbone (116,80 ± 11,28 t·ha-1) que les autres unités de végétation. La valeur du service écologique de séquestration du carbone dans la biomasse de la réserve écologique est estimée à 1 868 ·ha-1, soit 1 225 754 F CFA·ha-1, en utilisant la valeur du service écologique estimée par Ecosystem Marketplace.
Conclusions. La réserve écologique de Borotou-Koro, à travers ces types de végétation, séquestre des quantités de carbone et contribue ainsi à la réduction des gaz à effet de serre émis dans l’atmosphère.
Abstract
Structure and carbon stock of different vegetation types in the ecological reserve of Borotou-Koro in the West-Central region of Côte d'Ivoire
Description of the subject. Forest ecosystems play an important role in mitigating climate change by reducing carbon dioxide, a greenhouse gas.
Objectives. To describe the structural profile and to estimate carbon stocks in the vegetation types of the Borotou-Koro ecological reserve in Côte d'Ivoire.
Method. Data was collected in 30 plots of 2,500 m² (50 m x 50 m), delineated into three types of vegetation (riparian forest, open forest, and savannah) in the ecological reserve. Dendrometric measurements of diameter and height were carried out on all trees with dbh ≥ 5 cm, making it possible to determine the structural profile and estimate the biomass and corresponding carbon stock, using allometric equations, for each biotope.
Results. The open forest has the highest stand density (254 ± 60.44 stems·ha-1) and basal area (31.51 ± 10.57 m²·ha-1). The distribution of trees by diameter class in the three environments has the appearance of an inverted ‘J’ and is best fitted with polynomial functions. The ecological reserve sequesters a significant amount of carbon, estimated at 67.03 ± 12.89 t·ha-1. The open forest stores more carbon (116.80 ± 11.28 t·ha-1) than the other vegetation units. The value of the ecological service of carbon sequestration in the biomass of the ecological reserve is estimated at 1,868 €·ha-1, or 1,225,754 FCFA·ha-1, using the value of the ecological service estimated by Ecosystem Marketplace.
Conclusions. Through these types of vegetation, the Borotou-Koro ecological reserve sequesters quantities of carbon and plays a vital role in regulating the climate in the Worodougou region of Côte d'Ivoire.
Table des matières
Reçu le 23 octobre 2023, accepté le 25 février 2025, mis en ligne le 24 mars 2025.
Cet article est distribué suivant les termes et les conditions de la licence CC-BY (http://creativecommons.org/licenses/by/4.0/deed.fr)
1. Introduction
1Les forêts tropicales sont reconnues pour leur très grande diversité spécifique (Schroeder et al., 2010 ; Slik et al., 2015). Elles offrent de multiples services tels que le stockage et la purification de l’eau, l’atténuation des catastrophes naturelles et la séquestration du carbone (Gbozé et al., 2017). Selon Kervinio & Rais (2019), les forêts permettent de réguler le climat car elles contribuent significativement à la séquestration du carbone contenu dans le dioxyde de carbone émis chaque année dans l’atmosphère (49 Gt CO2). Par ailleurs, la dégradation du couvert végétal, par le biais des phénomènes anthropiques ou naturels, conduit à la libération dans l’atmosphère de quantités de carbone supérieures à celles utilisées par la végétation lors de la photosynthèse (Brown, 2002). Pour cela, Dimobe (2017) a montré qu’il est nécessaire de développer des stratégies qui font de la forêt un lieu de stockage de carbone plutôt qu’une source de production de carbone.
2Malheureusement, les forêts tropicales subissent des pressions grandissantes liées à la déforestation et à la dégradation forestière (Malhi et al., 2004). En Côte d’Ivoire, le processus de déforestation et de dégradation des forêts a entrainé une perte de la couverture végétale qui est passée de 16 millions d’hectares de forêts au début des années 1960 à 3,4 millions d’hectares en 2015 (MINEF, 2018). Les activités anthropiques comme les prélèvements incontrôlés des ressources forestières et l’agriculture extensive sur brûlis ont joué un rôle crucial dans la dégradation de ces écosystèmes, dans l’extinction des espèces végétales, animales et dans les changements climatiques (Ghazoul & Sheil, 2010).
3Face à cette problématique, un intérêt croissant se déploie en faveur de la mise en place de stratégies globales pour la conservation de la biodiversité et l’atténuation des changements climatiques dans les négociations internationales (Scheldeman & van Zonneveld, 2012). Dans ce contexte, le processus de Réduction des Émissions issues de la Déforestation et de la Dégradation des forêts (REDD) fut introduit en 2005 à la 11è Conférence des Parties (COP11) tenue à Montréal et révisé à la COP13 tenue à Bali en 2007 (Ilboudo, 2018). Comme d’autres pays, la Côte d’Ivoire s’est engagée depuis 2011 dans le processus REDD+ qui vise à réduire les émissions de gaz à effet de serre (GES) dues à la déforestation et à la dégradation des forêts. Ce processus inclut les rôles de conservation, de gestion durable des forêts et d’accroissement des stocks de carbone pouvant contribuer à la lutte globale contre le changement climatique (Gueulou et al., 2020).
4Dans cette dynamique, la Société Sucrivoire intervenant dans le domaine a adhéré au concept « agriculture zéro déforestation » en protégeant des zones HCS (High Carbon Stock) par la préservation de 150 ha de forêts dans le Centre-Ouest du pays pour en faire une réserve écologique. Cette réserve s’inscrit dans la dynamique de création des Réserves Naturelles Volontaires (RNV) en Côte d’Ivoire.
5Pour une utilisation durable des biens et services des RNV, la nécessité d’une gestion durable est primordiale (Jiagho, 2018) et cela, à travers la connaissance de la flore et du fonctionnement de son écosystème. Plusieurs travaux ont été réalisés dans ce sens, comme ceux effectués dans la forêt privée d’Allany dans la sous-préfecture de Rubino (Andji & Ettien, 2020), dans la réserve forestière de Dékpa à Divo (Vroh et al., 2016), dans le cadre de l’érection de la Forêt Sacrée Bokasso en une future RNV (Adou Yao et al., 2013) et dans la Forêt des Marais Tanoé-Ehy (Zadou et al., 2011).
6Pour la réserve écologique de Borotou-Koro, une étude a été menée en 2012 sur sa diversité faunistique et floristique en vue d’évaluer sa valeur pour la conservation et de déterminer son caractère particulier pour une RVN (Sucrivoire, 2012). Cependant, aucune étude sur le service écologique de la réserve n’a été entreprise jusqu’à ce jour. C’est en cela que cette étude trouve toute sa justification. Elle a pour objectif de mettre en relief le rôle écologique de la réserve forestière afin de justifier davantage sa conservation. L’hypothèse selon laquelle la quantité de carbone dans la biomasse des types de végétation de la réserve écologique de Borotou-Koro varie significativement entre ces types a été émise. De façon spécifique, il s’agit de :
7– déterminer les paramètres structuraux des types de végétation de la réserve forestière ;
8– d’estimer les stocks de carbone associés aux types de végétation et la valeur économique de cette réserve.
2. Matériel et méthodes
2.1. Description de la zone d’étude
9La réserve écologique du complexe sucrier de Borotou-Koro est située dans le Département de Séguéla, au Centre-ouest de la Côte d’Ivoire (Figure 1). Elle est inscrite dans le secteur subsoudanais selon la définition de Guillaumet (1967) cité par Kouamé (2010). Le climat soudanais est caractérisé par un régime pluviométrique de type monomodal (mai-octobre) avec une moyenne de 1 300 mm de précipitations par an et une température moyenne de 26,2 °C. Les sols sont de type ferralitique, généralement peu profonds, de texture sablo-argileuse et parsemés par endroits de plateaux constitués de sols granitiques. Le réseau hydrographique de la zone est composé de nombreux cours d’eau saisonniers, tous affluents du fleuve Sassandra (Anader, 2018). La végétation naturelle de ce secteur est essentiellement composée de formations savanicoles caractérisées par les espèces telles que Crossopteryx febrifuga (Afze. ex G.Don) Benth., Lophira lanceolata Tiegh. ex Keay, Terminalia avicennioides Guill. & Perr. et parsemées d’îlots de forêts claires formés d’espèces telles que Afzelia africana Sm. Ex Pers., Milicia excelsa (Welw.) C.C.Berg, Pterocarpus erinaceus Poir. et de forêts ripicoles le long des cours d’eau dont les principales espèces sont Cola laurifolia Mast., Manilkara multinervis Dubard, Pterocarpus santalinoides L'Hér. ex DC. (Sucrivoire, 2012).
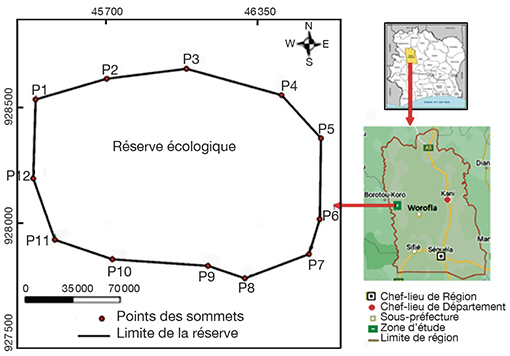
Figure 1. Localisation de la zone d’étude — Location of study area.
2.2. Collecte des données
10Pour la réalisation de l’étude, la méthode de l’inventaire de surface basée sur un échantillonnage stratifié a été utilisée. Le dispositif expérimental est inspiré de celui de Winrock International (2005) où l’estimation et le suivi du stock de carbone se font par la mise en place de parcelles permanentes ou temporaires. Les parcelles temporaires ont été utilisées puisque l’étude ne porte pas sur une analyse périodique des changements de la structure des types de végétation. L’approche phytosociologique basée sur des relevés effectués dans des parcelles de 2 500 m² (50 m x 50 m) a été appliquée pour les trois types de formations végétales qui composent la réserve écologique (Saradoum et al., 2022). Au total, 18 parcelles ont été disposées, ce qui équivaut à six parcelles par formation végétale. Dans chaque parcelle, des mesures dendrométriques ont été effectuées en vue d’apprécier l’état des structures et d’estimer la biomasse des populations de différentes communautés végétales. Pour ce faire, tous les individus ligneux de diamètre à hauteur de poitrine (DHP) ≥ 5 cm et de hauteur ≥ 2 m ont été mesurés en utilisant le ruban mètre (pour la circonférence) et le dendromètre électronique (pour la hauteur). L’identification de toutes les espèces ligneuses rencontrées dans les parcelles a été effectuée sur la base des travaux de Hutchinson & Dalziel (1972) révisés par Lebrun & Stork (1991, 1997).
2.3. Méthode d’analyse des données
11Analyse structurale de la végétation. Les données dendrométriques ont servi à faire l’analyse de la structure de la végétation. Cette analyse a porté sur les paramètres structuraux (densité de peuplement, diamètre moyen et surface terrière) et les distributions des individus des espèces par classe de diamètre et par classe de hauteur.
12Densité totale du biotope (D, tiges·ha-1) : ce paramètre a été calculé pour chaque biotope grâce à la formule mathématique suivante :
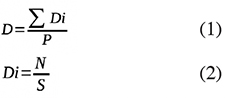
13où Di désigne la densité de peuplement de la placette i (tiges·ha-1), P est le nombre des placettes, N est le nombre d’individus de la placette et S est la surface d’observation rapportée en hectare.
14Diamètre quadratique moyen (Dm, cm) : Ce paramètre permet d’estimer le degré d’exploitation des gros arbres dans un biotope (Konan et al., 2015). Il se calcule par la formule suivante :

15où di est le diamètre à 1,30 m au-dessus du sol de l’arbre i du peuplement (cm) et N, le nombre total d’individus rencontrés dans le biotope.
16Hauteur moyenne (Hm, m) : Elle représente la moyenne des hauteurs des arbres dans un écosystème forestier. La hauteur moyenne se calcule par la formule suivante :

17où Hi est la hauteur de l’arbre i (m) et N, le nombre total d’individus dans le biotope.
18Surface terrière (G, m²·ha-1) : Ce paramètre traduit mieux l’occupation horizontale du sol par les espèces végétales et son évolution est caractéristique de la croissance d’un biotope (Rollet, 1974). Il se calcule par la formule suivante :

19où di est le diamètre de chaque individu (m) et S, la surface totale d’observation en hectare.
20Les histogrammes de distribution : ils ont été établis par classe de diamètre de 10 cm et par classe de hauteur de 4 m pour rendre compte de la structure démographique des peuplements ligneux de chaque type de végétation.
21Potentiel de séquestration du carbone et valeur économique
22Biomasse épigée ou aérienne par individu (Bai, t MS) : l'équation allométrique à trois prédicteurs développée par Chave et al. (2014) pour les climats tropicaux secs a été utilisée pour calculer la biomasse épigée de chaque individu.
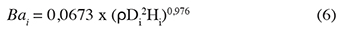
23où ρ est la densité spécifique du bois séché à 103 °C. Pour les espèces dont la densité spécifique n’est pas connue, une densité moyenne de ρ = 0,58 g·cm3 a été attribuée (Chave, 2005). D est le diamètre à hauteur de poitrine (cm) de l’arbre et H est la hauteur totale de l’arbre (m).
24Biomasse hypogée ou souterraine par individu (Bsi, t MS) : la biomasse épigée des ligneux recensés sert à déduire la biomasse hypogée selon l'équation allométrique développée par Cairns et al. (1997) cités par Tchobsala et al. (2016).
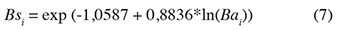
25Biomasse totale (Bt) des ligneux sur pied (Bt, t MS·ha-1) : la biomasse totale pour chaque unité de végétation est estimée à partir de la somme des biomasses aérienne et racinaire de l’ensemble des individus inventoriés pour chaque type de végétation. La biomasse totale de la réserve a été déterminée en sommant les quantités totales de biomasse obtenue pour tous les individus de chaque type de végétation. Par souci de simplification, les résultats ont été présentés en tonnes par hectare.

26où S est la surface totale d’observation en hectare.
27Stock de carbone des ligneux (SC, t C·ha-1) : les stocks du carbone par unité de surface des ligneux sont liés à la biomasse totale (Bt).

28où k = 0,487, correspondant au facteur de conversion de la biomasse en carbone par défaut (Guendehou et al., 2012).
29Stock de dioxyde de carbone par unité de surface (t CO2·ha-1) : il est obtenu en multipliant le stock de carbone par le ratio 44/12 (3,667) correspondant au rapport des masses moléculaires du CO2 et du C.
30Valeur économique de la réserve : les stocks de CO2 sont évalués en valeur monétaire en utilisant la valeur du service écologique estimé à 6,53 USD·téq CO2-1 (Ecosystem Marketplace, 2023).
2.4. Analyse statistique
31Les données quantitatives obtenues dans les différentes parcelles étudiées ont fait l’objet de diverses analyses via le logiciel XLSTAT.2016. L’analyse de variance (ANOVA) et le test de Kruskal-Wallis ont été utilisés pour vérifier le niveau de significativité des différences entre les variables calculées. Le test de Shapiro-Wilk a permis de vérifier la normalité de la distribution des données. Un test de corrélation a été aussi réalisé entre différentes grandeurs mesurées ou calculées, notamment le diamètre, la hauteur, la densité et les stocks de biomasse. Le niveau de significativité choisi pour ces analyses est de 5 % (p = 0,05).
3. Résultats
3.1. Caractéristiques structurales des formations végétales
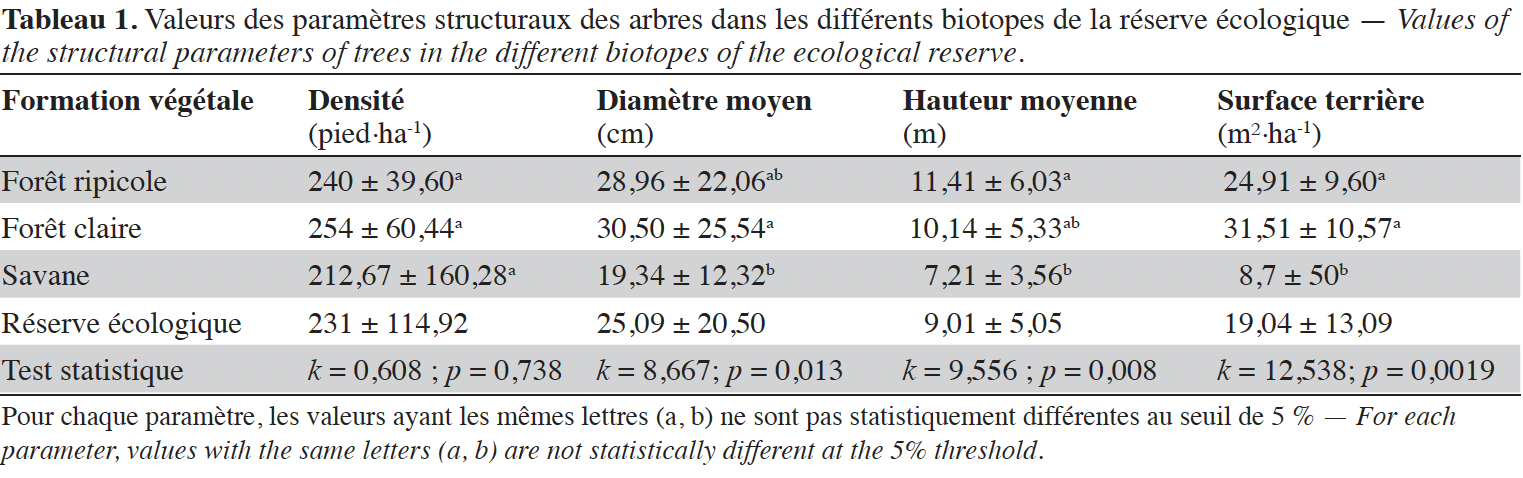
32L’analyse du tableau 1 permet de noter les valeurs des différents paramètres supérieurs pour les deux formations forestières comparées à la savane. La densité pour l’ensemble de la réserve écologique est estimée à 231 ± 114,92 pieds·ha-1. Concernant les biotopes, aucune différence significative n’a été observée entre les valeurs moyennes de la densité. Les valeurs ont varié de 254 ± 60,44 pieds·ha-1 pour les forêts claires à 212,67 ± 160,28 pieds·ha-1 pour les savanes (k = 0,608 ; p = 0,738). Pour le diamètre moyen, les forêts claires enregistrent la plus forte valeur moyenne (30,50 ± 25,54 cm) significativement supérieure à celle des savanes qui cumulent la plus faible valeur moyenne estimée à 19,34 ± 12,32 cm (k = 8,667 ; p = 0,013). Concernant la hauteur moyenne, une différence significative est observée entre les valeurs moyennes (k = 9,556 ; p = 0,008) des forêts ripicoles (11,41 ± 6,03 m) et des savanes (7,21 ± 3,56 m). La valeur moyenne de la surface terrière pour la savane est significativement inférieure à celle des deux forêts. La valeur la plus élevée de 31,51 ± 10,57 m²·ha-1 est observée dans la forêt claire, alors que la valeur la plus faible de 8,7 ± 50 m²·ha-1 est obtenue dans les savanes (k = 12,538 ; p = 0,0019).
33La figure 2 présente la distribution des arbres de dbh ≥ 5 cm par classes de diamètre. Cette distribution, obtenue pour chaque biotope, présente dans l’ensemble une forme polynomiale avec une allure en « J inversé », traduisant une forte représentativité des individus de petit diamètre et une absence des individus de grand diamètre, particulièrement dans les zones de savane. Les individus qui se situent dans les classes de diamètre [5-15 cm[ et [15-25 cm[ représentent plus de 50 % de la densité de peuplement des trois biotopes de la réserve écologique. Les savanes constituent le biotope qui concentre le plus grand nombre d’individus de diamètre compris entre 5 et 15 cm. La distribution de la surface terrière montre que, dans les forêts claires et ripicoles, les arbres de diamètres importants (75 à 85 et 105 à plus) cumulent l’essentiel de la surface terrière totale. Par contre, dans les savanes, une configuration différente est observée traduisant que les arbres de diamètre 25 à 35 cm cumulent l’essentiel de la surface terrière totale.
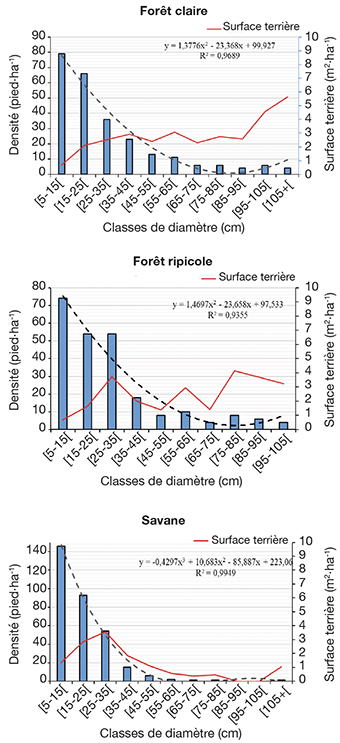
Figure 2. Distribution du nombre d’individus par classe de diamètre dans les biotopes de la réserve écologique — Distribution of the number of individuals by diameter class in the biotopes of the ecological reserve.
34La répartition des arbres inventoriés par classe de hauteur totale (Figure 3) présente une distribution en cloche asymétrique, orientée vers la gauche et centrée sur la classe de hauteur 6 m à 10 m, dans les forêts ripicoles et les forêts claires. Cette répartition des individus par classes de hauteur indique une configuration différente dans la zone de savane, traduisant une distribution en « J inversé » avec une prédominance des individus ayant une hauteur comprise entre 2 m et 6 m (Figure 3).
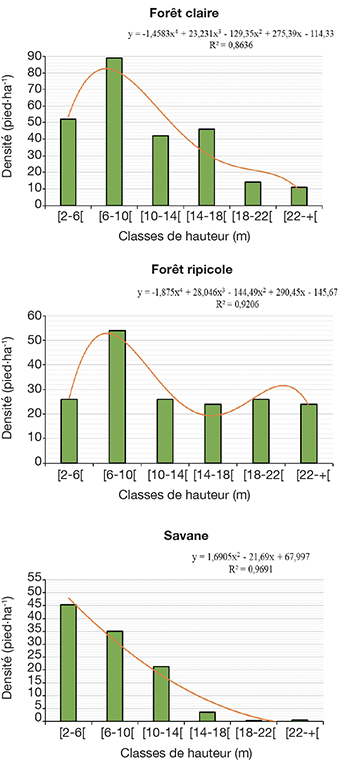
Figure 3. Distribution du nombre d’individus par classe de hauteur dans les biotopes de la réserve écologique — Distribution of the number of individuals per height class in the biotopes of the ecological reserve.
3.2. Biomasse et stock de carbone des formations végétales
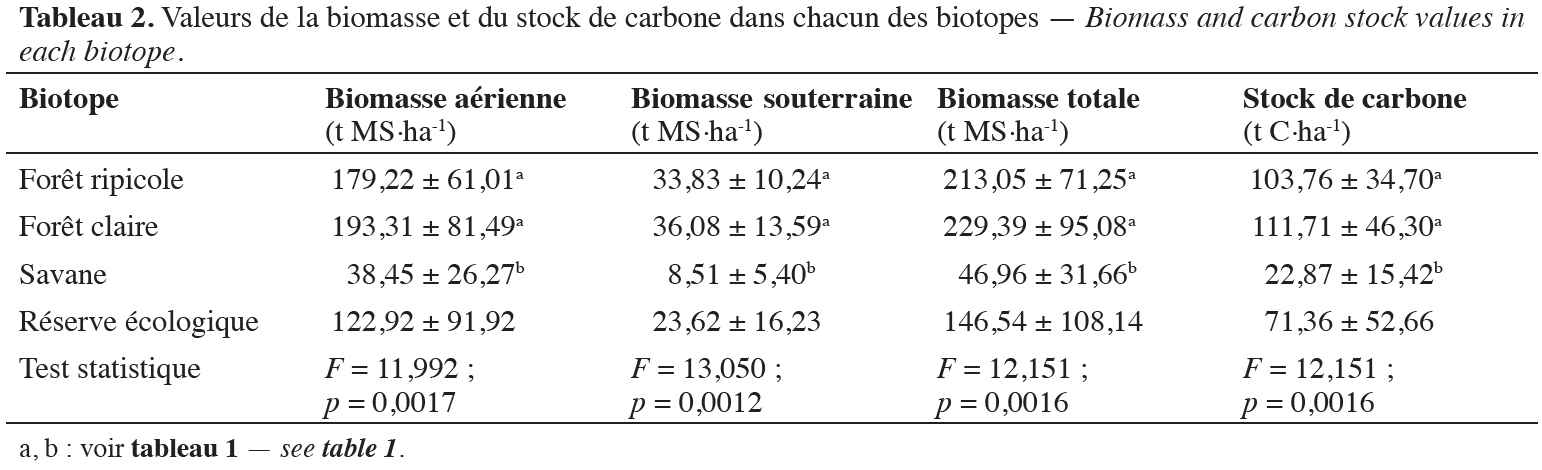
35Le stock de biomasse totale dans la réserve écologique est de 146,54 ± 108,14 t MS·ha-1, ce qui équivaut à 71,36 ± 52,66 t C·ha-1 de carbone. Le tableau 2 présente les détails relatifs aux valeurs de biomasse et de carbone dans les différentes unités de végétation de la réserve écologique. La forêt claire est le biotope qui enregistre la plus forte valeur de la biomasse totale estimée à 229,39 ± 95,08 t MS·ha-1, elle n’est pas significativement différente de la biomasse pour la forêt ripicole mais bien de la plus faible valeur de cette biomasse observée au niveau de la savane, avec 46,96 ± 31,66 t MS·ha-1 (F = 12,151 ; p = 0,0016). Pour le stock de carbone résultant de la biomasse, la forêt claire enregistre également la plus forte valeur moyenne avec 111,71 ± 46,30 t C·ha-1 et la savane enregistre la plus faible valeur qui est de 22,87 ± 15,42 t C·ha-1 (F = 12,151 ; p = 0,0016)).
36La figure 4 présente la répartition de la biomasse totale en classes de diamètre dans les biotopes de la réserve forestière. Il ressort que la biomasse est plus importante dans les classes des diamètres les plus importants (> 75 cm) dans les zones de forêt. Au niveau de la forêt claire, la classe diamétrique [105 cm-+[ a une quantité de biomasse très élevée et très faible dans l'intervalle de [5-15 cm[. Dans la forêt ripicole, la classe diamétrique 75-85 cm a une quantité de biomasse très importante et très faible dans la classe diamétrique 5-15 cm. Par contre, la zone savanicole stocke une quantité importante de biomasse dans la classe de diamètre 25-35 cm et une quantité faible dans la classe de diamètre 65-75 cm.
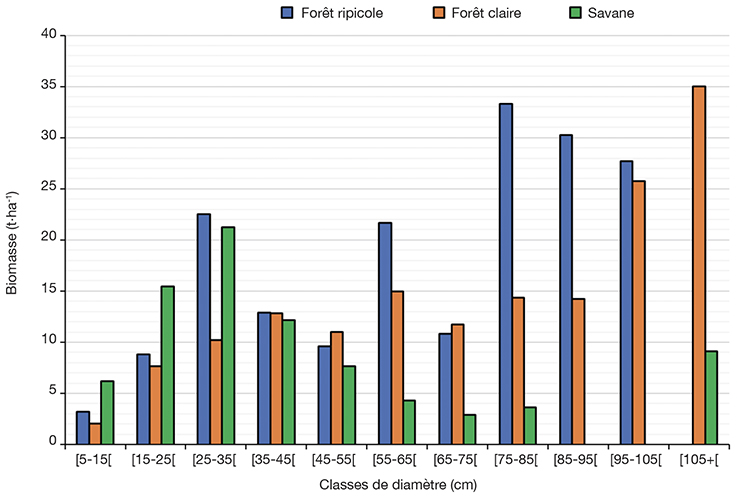
Figure 4. Répartition de la biomasse totale en fonction des classes de diamètre dans les types de biotopes — Distribution of total biomass according to diameter classes in biotope types.
3.3. Contribution des espèces inventoriées à la biomasse végétale et au potentiel de séquestration du carbone
37La contribution spécifique à la quantité de biomasse et au stock de carbone par unité de surface (en ha), n’est pas la même pour toutes les espèces dans la réserve (Tableau 3). Concernant la contribution liée à la densité spécifique, Ceiba pentandra (L.) Gaertn. est l’espèce ayant la plus forte quantité de biomasse, avec 22,35 t MS·ha-1, correspondant à 10,88 t C·ha-1de carbone. Elle est suivie de Afzelia africana Sm. & Pers. (11,32 t MS·ha-1 de biomasse et 5,51 t C·ha-1 de carbone), de Cola cordifolia (Cav.) R.Br. (9,97 t MS·ha-1 de biomasse et 4,85 t C·ha-1 de carbone), de Diospyros mespiliformis Hochst. ex A.DC. (9,26 t MS·ha-1 de biomasse et 4,51 t C·ha-1 de carbone), de Pterocarpus erinaceus Poir. (8,75 t MS·ha-1 de biomasse et 4,26 t C·ha-1 de carbone ) et enfin de Terminalia leiocarpa (DC.) Baill. (8,16 t MS·ha-1 de biomasse et 3,97 t C·ha-1 de carbone). Ces six espèces représentent à elles seules 53,85 % de la quantité de la biomasse de la réserve écologique du complexe sucrier de Borotou-Koro.
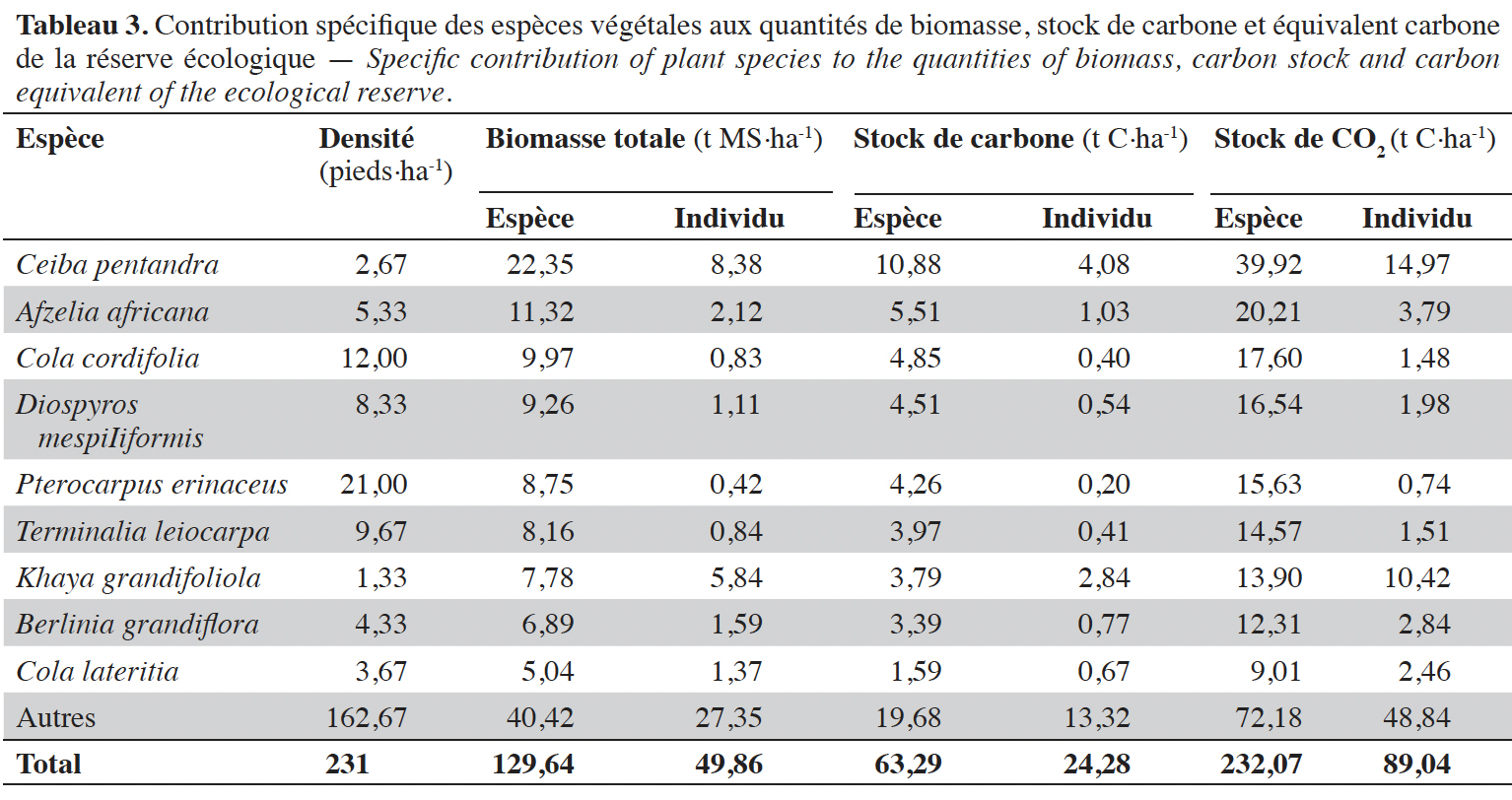
38Lorsque les quantités de biomasse et de carbone correspondant sont estimées, en tenant compte de leur DBH, C. pentandra est également l’espèce qui renferme les individus les plus productifs avec 8,38 t MS·ha-1·pied-1 de biomasse en moyenne sur l’ensemble des individus, pour un stock de carbone de 4,08 t C·ha-1·pied-1. La seconde place est occupée par Khaya grandifoliola C.DC. avec une quantité de biomasse en moyenne sur l’ensemble des individus de 5,84 t MS·ha-1·pied-1, soit un stock de carbone de 2,84 t C·ha-1·pied-1. Suivent A. africana (2,12 t MS·ha-1·pied-1 ; 1,03 t C·ha-1·pied-1), Berlinia grandiflora (Vahl) Hutch. & Dalziel (1,59 t MS·ha-1·pied-1 ; 0,77 t C·ha-1·pied-1), C. lateritia (1,37 t MS·ha-1·pied-1 ; 0,67 t C·ha-1·pied-1) et D. mespiIiformis avec 1,11 t MS·ha-1·pied-1, soit 0,54 t C·ha-1·pied-1 (Tableau 3).
3.4. Stock du dioxyde de carbone et valeur économique dans les formations végétales
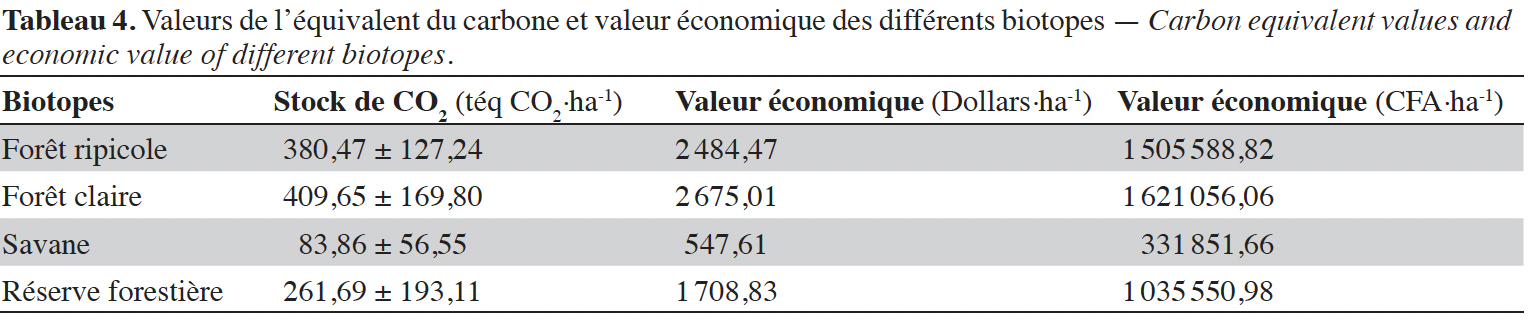
39Le stock de CO2 est plus important dans les forêts claires que dans les autres formations végétales avec une valeur moyenne de 409,65 ± 169,80 téq CO2·ha-1. Ce stock de dioxyde de carbone représente une valeur financière de 2 675,01 dollars·ha-1 soit 1 621 056,06 F CFA·ha-1. Pour la savane, qui enregistre la plus faible valeur du stock de dioxyde de carbone (83,86 ± 56,55 téq CO2·ha-1), la valeur financière du potentiel de séquestration est évaluée à 547,61 dollars·ha-1, soit 331 851,66 F CFA·ha-1 (Tableau 4).
3.5. Corrélation entre les paramètres dendrométriques et la biomasse totale
40La corrélation entre la quantité de biomasse et le diamètre des arbres de la réserve écologique est forte et significative en ce qui concerne la biomasse totale (F = 5,534 ; p ˂ 0,010 ; r² = 0,542). Il existe également une corrélation significative entre la quantité de biomasse et la hauteur moyenne des arbres (F = 6,325 ; p ˂ 0,006 ; r² = 0,575), ce qui signifie que les quantités de biomasse produites par les types de végétation de la réserve écologique sont corrélées aux diamètres et à la taille des arbres. Par contre, il n’existe pas de corrélation entre les quantités de biomasse dans les biotopes et la densité de peuplement (F = 0,227 ; p ˂ 0,875 ; r² = 0,046), ce qui signifie que les quantités de biomasse des biotopes ne sont pas corrélées au nombre des individus des espèces végétales inventoriées dans les types de végétation (Figure 5).
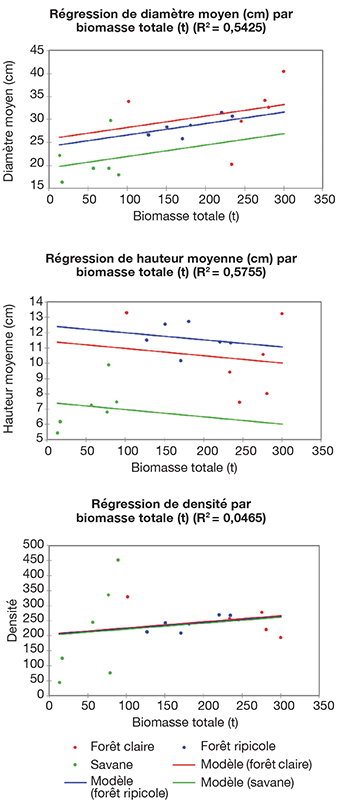
Figure 5. Corrélation entre le diamètre, la hauteur, la densité et les stocks de biomasse dans les différents biotopes — Correlation between diameter, height, density and biomass stocks in different biotopes.
4. Discussion
41Les paramètres structuraux (densité de peuplement, diamètre moyen, hauteur moyenne et surface terrière) dans la réserve écologique du complexe sucrier de Borotou-Koro varient d’un biotope à un autre, avec des différences parfois significatives. Les différences, au niveau de ces paramètres, sont principalement observées entre les milieux des savanes et ceux des forêts. Cela résulte naturellement des processus dynamiques des conditions écologiques qui existent dans ces milieux. En effet, les milieux de forêts sont plus humides que ceux des savanes, ce qui représente un facteur essentiellement important pour le développement des arbres. La variation des paramètres structuraux dans les zones de mosaïques forêts-savanes a été démontrée par plusieurs chercheurs (Adjonou et al., 2010 ; Woegan et al., 2011 ; Natta et al., 2012). La distribution par classe de diamètre des individus des biotopes décrit une allure en « j inversé », caractéristique des formations naturelles dont les peuplements se distinguent par une distribution stable des classes d’âge marquées par un nombre important de petites plantes et une faible représentation de grands arbres (Wala et al., 2005 ; Adrika et al., 2015).
42Les équations allométriques adoptées dans la présente étude ont permis de conclure que les quantités de biomasse varient significativement entre les formations forestières (forêt claire : 229,39 ± 95,08 t MS·ha-1 ; forêt ripicole : 213,05 ± 71,25 t MS·ha-1) et la savane (46,96 ± 31,66 t MS·ha-1) (Tableau 1). Les fortes valeurs de la biomasse dans ces formations forestières témoignent de l’existence de gros spécimens d’arbres. La corrélation significative entre le diamètre et la quantité de biomasse enregistrée corroborent les résultats de plusieurs auteurs concernant la contribution des individus de gros diamètres (M’Bow, 2009 ; Mille & Louppe, 2015). Les stocks de carbone correspondant aux quantités de biomasse estimées pour les forêts claires, les forêts ripicoles et pour les savanes sont en adéquation avec les résultats obtenus par Zakari et al. (2022) relatifs aux forêts et savanes de la forêt classée des Monts Kouffé au Centre-Bénin.
43En ce qui concerne la contribution spécifique des espèces à la présence de biomasse végétale dans la réserve écologique, cinq espèces se sont révélées les plus importantes : Ceiba pentandra, Afzelia africana, Pterocarpus erinaceus, Diospyros mespiliformis et Cola cordifolia. Il s’agit essentiellement d’espèces inféodées aux savanes soudanaises en Côte d’Ivoire. Par contre, après estimation de la biomasse par individu de chaque espèce, les espèces locales telles que Ceiba pentandra, Khaya grandifoliola, Triplochiton scleroxylon, Isoberlinia doka, Afzelia africana et Morus mesozygia sont celles qui possèdent les arbres produisant les plus fortes quantités de biomasse et de carbone séquestré. Il est important de souligner qu'il s'agit en général d’essences forestières couramment utilisées en exploitation forestière. Ces différents résultats corroborent ceux de Tsoumou et al. (2016) qui ont montré que le stock de carbone dépend principalement des essences forestières qui la composent et des classes de diamètre.
44L’évaluation des stocks de biomasses et de carbone correspondant est indispensable à la mise en œuvre des stratégies d’atténuation des changements climatiques que prône le mécanisme de réduction des émissions dues à la déforestation et à la dégradation (REDD+). Pour l’ensemble des biotopes de la réserve écologique, les estimations de l’équivalent carbone sont de 71,36 ± 52,66 t C·ha-1. La préservation de la destruction de ces arbres à cause de la mise en place de la culture de canne à sucre empêcherait les émissions de CO2 dans l’atmosphère. Des résultats similaires ont été obtenus dans les unités de végétation de la forêt classée des Monts Kouffé au Bénin par Zakari et al. (2022). La vente du carbone permettrait de bénéficier de 1 868 €·ha-1, soit 1 225 754 F CFA·ha-1. Ces bénéfices monétaires issus de la vente du carbone font de la réserve écologique de Borotou-Koro un potentiel candidat au processus REDD+ en Côte d’Ivoire.
5. Conclusions
45L’étude menée dans la réserve écologique du complexe sucrier de Borotou-Koro sur les caractéristiques structurales et le potentiel de séquestration du carbone met en évidence des différences statistiquement significatives au niveau des paramètres calculés entre les types de végétation, particulièrement entre les formations forestières et celles de savane. La forêt claire est le biotope qui possède les plus fortes valeurs de paramètres structuraux, de quantités de biomasse et de stockage de carbone correspondant, bien qu’aucune différence significative n’ait été observée avec la forêt ripicole. La structure diamétrique des types de végétation est dominée par les tiges de petites classes de diamètre, capables d’assurer leur reconstitution si des mesures idoines de mise en défens sont entreprises. Aussi, les biotopes de la réserve écologique séquestrent une quantité de CO2 estimée à 261,69 ± 193,11 t CO2·ha-1. Les essences forestières dont les individus sont de gros spécimens concentrent de fortes quantités de biomasse et de carbone séquestré. Ces espèces de bois d’œuvre constituent un réservoir important de stockage de carbone dans les unités de végétation. Il convient donc de mettre en place une politique de conservation de ces espèces en particulier et des écosystèmes qui les abritent en général afin que la réserve écologique puisse jouer pleinement son rôle de préservation écologique de réservoir de carbone dans le cadre de la lutte contre le réchauffement climatique.
Remerciements
46Les auteurs remercient la Banque Islamique de Développement (BID) pour l’appui financier et les responsables du complexe sucrier de Borotou-Koro pour l’appui technique apportés à la réalisation de la présente étude.
Bibliographie
Adjonou K. et al., 2010. Étude de la dynamique spatiale et structure des forêts denses sèches reliques du Togo : implications pour une gestion durable des aires protégées. Int. J. Biol. Chem. Sci., 4(1), 168-183, doi.org/10.4314/ijbcs.v4i1.54242
Adou Yao C.Y. et al., 2013. Diversité floristique et valeur de la forêt sacrée Bokasso (Est de la Côte d’Ivoire) pour la conservation. VertigO, 13(1), doi. org/10.4000/vertigo.13500
Adrika N.B.T. & Lare L.Y., 2015. Caractéristiques des groupements végétaux saxicoles du plateau de Soudou-Dako dans la chaîne de l’Atakora au Togo. Notes Sci. Homme Soc., 3, 203-223
Anader Z.S., 2018. Monographie de la région de Séguéla. Séguéla, Côte d’Ivoire.
Andji H.N. & Etien D.T., 2020. Évaluation de la flore et des stocks de carbone dans une forêt privée à Allany (Rubino - Cote d’Ivoire). Agron. Afr., 32(4), 475-488.
Brown S., 2002. Measuring carbon in forests: current status and future challenges. Environ. Pollut., 116(3), 363-372, doi.org/10.1016/s0269-7491(01)00212-3
Cairns M.A., Brown S., Helmer E.H. & Baumgardner G.A., 1997. Roots biomass allocation in the world’s upland forests. Oecologia, 111, 1-11, dx.doi.org/10.1007/s004420050201
Chave J., 2005. Measuring wood density for tropical forest trees, 1-7. Retrieved from Chave J. et al., 2014. Improved allometric models to estimate the aboveground biomass of tropical trees. Global Change Biol., 20, 3177-3190, doi.org/10.1111/gcb.12629
Dimobe K., 2017. Dynamique, séquestration de carbone et modèles de variations des savanes soudaniennes du Burkina Faso et du Ghana (Afrique de l’Ouest). Thèse de doctorat : Université Joseph Ki-Zerbo, Ouagadougou (Burkina Faso).
Ecosystem Marketplace, 2023. New report: the voluntary carbon market contracted in 2023, driven by drop-off in transactions for REDD+ and renewable energy, https://www.ecosystemmarketplace.com/articles/report-the-voluntary-carbon-market-contracted-in-2023-driven-by-drop-off-in-transactions-for-redd-and-renewable-energy/, (20/03/2025).
Gboze A.E., Coulibaly B., Kassi J. & N’Guessan K.A., 2017. Évaluation de la flore et des stocks de carbone de la forêt relique du site de la Direction Régionale d’Abidjan du CNRA (Côte d’Ivoire). Eur. J. Sci. Res., 147(2), 219-231.
Ghazoul J. & Sheil D., 2010. Tropical rain forest ecology, diversity, and conservation. Oxford, UK: University Press.
Guendehou G.H.S. et al., 2012. Stem biomass and volume models of selected tropical tree species in West Africa. South. For., 74(2), 77-88, doi.org/10.2989/20702620.2012.701432
Gueulou N. et al., 2020. Évaluation de la couverture forestière et du stock de carbone forestier de la réserve scientifique de Lamto (Côte d’Ivoire). Int. J. Innovation Appl. Stud., 28(3), 682-689.
Guillaumet J.L., 1967. Recherches sur la végétation et la flore de la région du Bas-Cavally (Côte d'Ivoire). Paris : ORSTOM.
Hutchinson J. & Dalziel J.M., 1972. Flora of West Tropical Africa. 2nd ed. Millbank, London: Crown Agents for Overseas Governments and Administrations.
Ilboudo D., 2018. Évaluation de la biomasse et du potentiel de séquestration de carbone par les petites formations forestières des savanes en zone soudanienne du Burkina Faso : cas du site de l’école Nationale des Eaux et Forêts (ENEF). Mémoire de fin de cycle de DEA : Université Nazi Boni, Ouagadougou (Burkina Faso).
Jiagho E.R., 2018. Flore et végétation ligneuse à la périphérie du Parc National de Waza (Cameroun), dynamiques et implications pour une meilleure gestion. Thèse de doctorat : Université de Yaoundé I (Cameroun)/Université du Mans (France).
Kervinio Y. & Rais A.C., 2019. La séquestration de carbone par les écosystèmes en France : une évaluation du service de séquestration in situ du carbone. Paris : EFESE.
Konan D. et al., 2015. Dynamisme de la structure diamétrique du peuplement ligneux des différents biotopes de la forêt classée de Yapo-Abbé, sud de la Côte d’Ivoire. J. Appl. Biosci., 94, 8869-8879, doi.org/10.4314/jab.v93i1.10
Kouamé N.F., 2010. Les territoires phytogéographiques. In : Konaté S. & Kampmann D., eds. Atlas de la biodiversité de l’Afrique de l’Ouest. Tome III : Côte d’Ivoire. Abidjan & Frankfurt/Main.
Lebrun J.P. & Stork A.L., 1991. Énumération des plantes à fleurs d'Afrique tropicale. Vol. 1 : généralités et Annonaceae à Pandaceae. Genève, Suisse : Conservatoire et Jardins Botaniques de la Ville de Genève.
Lebrun J.P. & Stork A.L., 1997. Énumération des plantes à fleurs d'Afrique tropicale. Vol. 4 : Gamopétales : Ericaceae à Lamiaceae. Genève, Suisse : Conservatoire et Jardins Botaniques de la Ville de Genève.
M’Bow C., 2009. Potentiel et dynamique des stocks de carbone des savanes soudaniennes et soudano- guinéennes du Sénégal. Thèse de doctorat : Université Cheikh Anta Diop de Dakar (Sénégal).
Malhi Y. et al., 2004. The above-ground coarse wood productivity of 104 Neotropical forest plots. Global Change Biol., 10(5), 563-591, doi.org/10.1111/j.1529-8817.2003.00778.x
Mille G. & Louppe D., 2015. Mémento du forestier tropical. Versailles, France : Éditions Quæ.
MINEF (Ministère des Eaux et Forêts), 2018. Stratégie Nationale de Préservation, de Réhabilitation et d’Extension des Forêts. Abidjan : MINEF.
Natta A.K., Wallis N.Z. & Dicko A., 2012. Typologie et structure des parcs agroforestiers dans la zone soudanienne du nord Bénin. Ann. Sci. Agron., 16(1), 67-90, https://www.ajol.info/index.php/asab/article/view/106720
Rollet B., 1974. L’architecture des forêts denses humides sempervirentes de plaines. Paris : Centre Technique Forestier Tropical.
Saradoum G. et al., 2022. Estimation du potentiel de séquestration de carbone des aires protégées : cas de la Forêt Classée de Djoli-Kera, Tchad. VertigO, doi.org/10.4000/vertigo.34658
Scheldeman X. & Van Zonneveld M., 2012. Manuel de formation à l’analyse spatiale de la diversité et de la distribution des plantes. Rome : Bioversity International.
Schroeder J.M., Oke D.O., Onyekwelu J.C. & Yirdaw E., 2010. Secondary forests in West Africa: a challenge and opportunity for management. In: Mery G. et al., eds. Forests and society - responding to global drivers of change. Vienna: IUFRO, 335-353.
Slik F.J.W.S. et al., 2015. An estimate of the number of tropical tree species. Proc. Natl Acad. Sci., 112, 7472-7477, doi.org/10.1073/pnas.1423147112
Sucrivoire, 2012. Évaluation de la diversité faunistique et floristique des reliques forestières des domaines de sucrivoire à Borotou-koro et à Zuenoula. Rapport d’étude. Abidjan : Sucrivoire.
Tchobsala Dongock N.D., Nyasiri J. & Ibrahima A., 2016. Carbon storage of anthropoid's vegetation on the Ngaoundéré escarpment (Adamawa, Cameroon). J. Adv. Biol., 9(2), 1845-1854, doi.org/10.24297/jab.v9i2.4012
Tsoumou B.R., Lumandé K.J., Nzila J.D. & Kampé J.P., 2016. Estimation de la quantité de carbone séquestré par la forêt modèle de Dimonika (sud-ouest de la République du Congo). Rev. Sci. Techn. For. Environ. Bassin Congo, 6, 39-45, doi.org/10.5281/zenodo.48399
Vroh B.T.A. et al., 2016. Un cas de compensation écologique dans le secteur minier : la réserve forestière Dékpa (Côte d'Ivoire) au secours des forêts et des populations locales. Environ. Ingénierie Développement, 72, 1-9, doi.org/10.4267/dechets-sciences-techniques.3511
Wala K. et al., 2005. Typologie et structure des parcs agroforestiers dans la préfecture de Doufelgou (Togo). Sécheresse, 16(1), 209-216, http://geoprodig.cnrs.fr/items/show/183867
Winrock International, 2005. Exploration du potentiel de séquestration du carbone dans les forêts classées de la République de Guinée. Guide de mesure et de suivi du carbone dans les forêts et prairies herbeuses. Little Rock, AR, USA : Winrock International.
Woegan Y.A., Akpavi S. & Dourma M., 2011. Diversité des formations végétales ligneuses du Parc national de Fazao-Malfakassa et de la réserve d’Alédjo (Togo). Acta Bot. Gallica, 158, 445-449, doi.org/10.1080/12538078.2011.10516286
Zadou D.A. et al., 2011. Valeur de la Forêt des Marais Tanoé-Ehy (Sud-Est de la Côte d’Ivoire) pour la conservation : dimension socio-anthropologique. Trop. Conserv. Sci., 4(4), 373-385, http://tropicalconservationscience.mongabay.com/content/v4/2011_dec_373-385_Zadou.pdf
Zakari S. et al., 2022. Potentiel de séquestration du carbone des formations forestières dans la forêt classée des Monts-Kouffé au Centre-Benin. Espace Géogr. Soc. Marocaine, 56, 195-213, doi.org/10.34874/IMIST.PRSM/EGSM/30087






