Caractérisation de la distribution spatiale de Prioria balsamifera (Vermoesen) Breteler et Prioria oxyphylla (Harms) Breteler dans la Réserve Forestière de Yoko (République Démocratique du Congo)
Résumé
Description du sujet. L’étude de la distribution spatiale des arbres apporte des informations sur l’écologie des espèces et la dynamique forestière. Sa connaissance est importante pour la gestion durable des grands arbres africains dont Prioria balsamifera (Vermoesen) Breteler et Prioria oxyphylla (Harms) Breteler font partie.
Objectifs. Cette étude visait à (i) caractériser le modèle de distribution spatiale de P. balsamifera et P. oxyphylla, (ii) mettre en évidence leurs relations intraspécifiques et interspécifiques et (iii) identifier les facteurs environnementaux pouvant expliquer leur structure spatiale.
Méthode. La fonction de corrélation par paires univariée et bivariée a été utilisée pour caractériser le modèle de distribution spatiale. Le modèle linéaire généralisé avec une distribution de Poisson et le test de randomisation par translation toroïdale ont permis de mettre en évidence les effets des facteurs environnementaux sur la structure spatiale de Prioria.
Résultats. Chaque espèce de Prioria présente une structure spatiale agrégée et une autocorrélation spatiale des diamètres des troncs, tout en partageant un même micro-habitat. Leur coexistence pourrait être facilitée par la différenciation de traits fonctionnels, P. balsamifera et P. oxyphylla présentant, respectivement, des stratégies acquisitive et conservatrice des ressources. Il existe une attraction entre les jeunes et les adultes de P. balsamifera dans un rayon de 500 m ; une tendance moins marquée chez P. oxyphylla. Enfin, l’abondance des individus de P. balsamifera et P. oxyphylla est significativement liée à l’altitude.
Conclusions. Cette étude montre que la distribution spatiale de ces deux espèces de Prioria est liée à l’altitude et leur coexistence est facilitée par une certaine différenciation de niche écologique.
Abstract
Characterization of the spatial distribution of Prioria balsamifera (Vermoesen) Breteler and Prioria oxyphylla (Harms) Breteler in the Yoko Forest Reserve (Democratic Republic of Congo)
Description of the subject. The study of the spatial distribution of trees provides information on species ecology and forest dynamics. Such knowledge is important for the sustainable management of large African trees, including Prioria balsamifera (Vermoesen) Breteler and Prioria oxyphylla (Harms) Breteler.
Objectives. This study aimed to (i) characterize the spatial distribution patterns of P. balsamifera and P. oxyphylla, (ii) highlight their intraspecific and interspecific relationships, and (iii) identify environmental factors that may explain their spatial structure.
Method. Univariate and bivariate pair correlation functions were used to characterize spatial distribution patterns. Generalized linear models with a Poisson distribution, together with toroidal shift randomization tests, were applied to assess the effects of environmental factors on the spatial structure of Prioria.
Results. Each Prioria species exhibits an aggregated spatial structure and spatial autocorrelation of trunk diameters, while sharing the same microhabitat. Their coexistence may be facilitated by functional trait differentiation, with P. balsamifera and P. oxyphylla displaying acquisitive and conservative resource-use strategies, respectively. An attraction between juveniles and adults of P. balsamifera was observed within a 500 m radius, with a less pronounced trend in P. oxyphylla. Finally, the abundance of individuals of both P. balsamifera and P. oxyphylla is significantly related to altitude.
Conclusions. This study shows that the spatial distribution of these two Prioria species is linked to altitude, and that their coexistence is facilitated by some degree of ecological niche differentiation.
Reçu le 11 avril 2025, accepté le 28 janvier 2026, mis en ligne le 24 février 2026.
Cet article est distribué suivant les termes et les conditions de la licence CC-BY (http://creativecommons.org/licenses/by/4.0/deed.fr)
1. INTRODUCTION
1La forêt tropicale dense humide d'Afrique centrale est l'un des biomes les plus riches en espèces au monde (Grantham et al., 2020). Elle est également très productive et séquestre beaucoup de carbone par rapport à d'autres forêts tropicales (Brienen et al., 2015; Hubau et al., 2020). Malheureusement, cette forêt subit des pressions tendant à la disparition de certaines espèces (Gemerden et al., 2003). C’est notamment le cas de Pycnocoma subflava J.Léonard et Vepris mandangoana Lisowski qui sont placées sur la liste rouge de l’UICN comme espèces en danger critique d’extinction car leurs habitats sont menacés par l’agriculture itinérante et l’exploitation forestière sélective (Sosef et al., 2021).
2L'étude de la distribution spatiale des espèces d'arbres est importante pour retracer l'empreinte des événements passés ayant concouru à leur installation (Luambua et al., 2021). À une échelle locale, trois modèles de distribution spatiale peuvent apparaître dans une communauté végétale : aléatoire, agrégée ou régulière (Réjou-Méchain et al., 2011).
3En écologie des populations et des communautés végétales, les liens entre les schémas de distribution et les facteurs qui les déterminent restent une question fondamentale (Fibich et al., 2016). Parmi les facteurs qui déterminent la distribution spatiale des espèces en forêt à une échelle locale, figurent l’hétérogénéité environnementale, la dispersion limitée des diaspores, les interactions positives ou négatives intraspécifiques ou interspécifiques et les perturbations passées ou actuelles (Ripley, 1987).
4L’hétérogénéité environnementale peut créer une agrégation pour certaines espèces (Ripley, 1987 ; Condit et al., 2013 ; Luambua et al., 2021). Par exemple, les espèces héliophiles ont tendance à s’installer dans les trouées de la canopée ou les perturbations forestières (Altman et al. 2016 ; Fibich et al., 2016). Par ailleurs, plusieurs études ont révélé les effets de la variation des propriétés du sol sur la structure spatiale de nombreuses espèces dans les forêts tropicales (Newbery et al., 1986 ; Morneau, 2007 ; Réjou-Méchain et al., 2008 ; Vleminckx et al., 2015). Dans une étude réalisée dans la réserve de Douala-Edea au Cameroun, Newbery et al. (1986) ont montré que des espèces comme Guibourtia demeusei (Harms) J.Léonard, Casearia stipitata Mast. et Maprounea membranacea Pax & K.Hoffm. étaient inféodées aux sols bien drainés et pauvres en phosphore.
5Les contraintes de dispersion (modes de dispersion) peuvent également influencer les modèles de distribution spatiale des espèces (Hardy & Sonké, 2004). La dispersion limitée des diaspores des espèces autochores explique que les individus ont tendance à s'agréger à de petites échelles spatiales et autour des pieds mères (Hardy & Sonké, 2004 ; Réjou-Méchain et al., 2011 ; Kumba et al., 2013).
6Les interactions négatives (par exemple, la compétition intraspécifique) peuvent engendrer une distribution régulière, alors que les interactions positives au sein d’une même espèce peuvent engendrer l'agrégation spatiale (Boulangeat et al., 2012 ; De Araújo et al., 2014). Nous n’avons toutefois pas connaissance d’espèces d’arbres présentant des distributions régulières en forêt tropicale humide.
7Des agents pathogènes fongiques, des insectes et des prédateurs des graines et plantules peuvent provoquer une mortalité élevée des semis et des graines en forte densité ou une mortalité dépendante de la distance aux pieds mères chez certaines espèces (Janzen, 1970 ; Connell, 1971 ; Levi et al., 2019 ; Terborgh, 2020). Cette mortalité modifie la répartition initiale des graines et conduit à l’éloignement des semis et des pieds mères, un phénomène souvent mentionné comme l’effet Janzen-Connell. Le recrutement se fait alors à l’extérieur des limites de la couronne des pieds mères (Janzen, 1970 ; Connell, 1971 ; Collinet, 1997). Cette situation serait liée au mode de dispersion des graines (Howe, 1989). Par exemple, les espèces autochores et certaines zoochores dont les graines sont capables de développer des adaptations de défenses chimiques ou mécaniques contre les facteurs de mortalité dépendante de la densité ont des zones de recrutements qui peuvent se situer directement sous le pied mère ou en limite de couronne. Ces espèces forment ainsi des agrégats denses. Cependant, les espèces anémochores, ayant une dispersion des graines éparpillées, ne développant aucun mécanisme de résistance aux causes de mortalité dépendante de la densité, ont des individus rarement recrutés sous le pied mère mais plutôt au-delà des limites des couronnes des adultes conspécifiques. Ils forment de faibles densités ou restent isolés dans des sites favorables (Howe, 1989).
8Les espèces du genre Prioria sont largement exploitées, par exemple en République Démocratique du Congo (RDC), par les entreprises d’exploitation forestière mais aussi par les bûcherons artisanaux pour la fabrication des pirogues (Bbidjo et al., 2024). Cependant, ces espèces ne sont pas suffisamment étudiées pour mettre en place des plans de gestion adéquats en vue de leur gestion durable. Il est donc nécessaire de comprendre l'écologie de ces espèces en forêt naturelle. Cette étude se focalise sur la distribution spatiale de deux espèces : Prioria balsamifera (Vermoesen) Breteler et Prioria oxyphylla (Harms) Breteler. Leurs structures spatiales sont décrites comme non grégaires au Gabon (Meunier et al., 2015) et variables selon les régions en République Démocratique du Congo (Shaumba, 2009 ; Kidikwadi et al., 2015). Par ailleurs, jusqu’à présent, aucune étude visant à identifier les facteurs qui définissent leurs modèles de distribution spatiale n’a été réalisée.
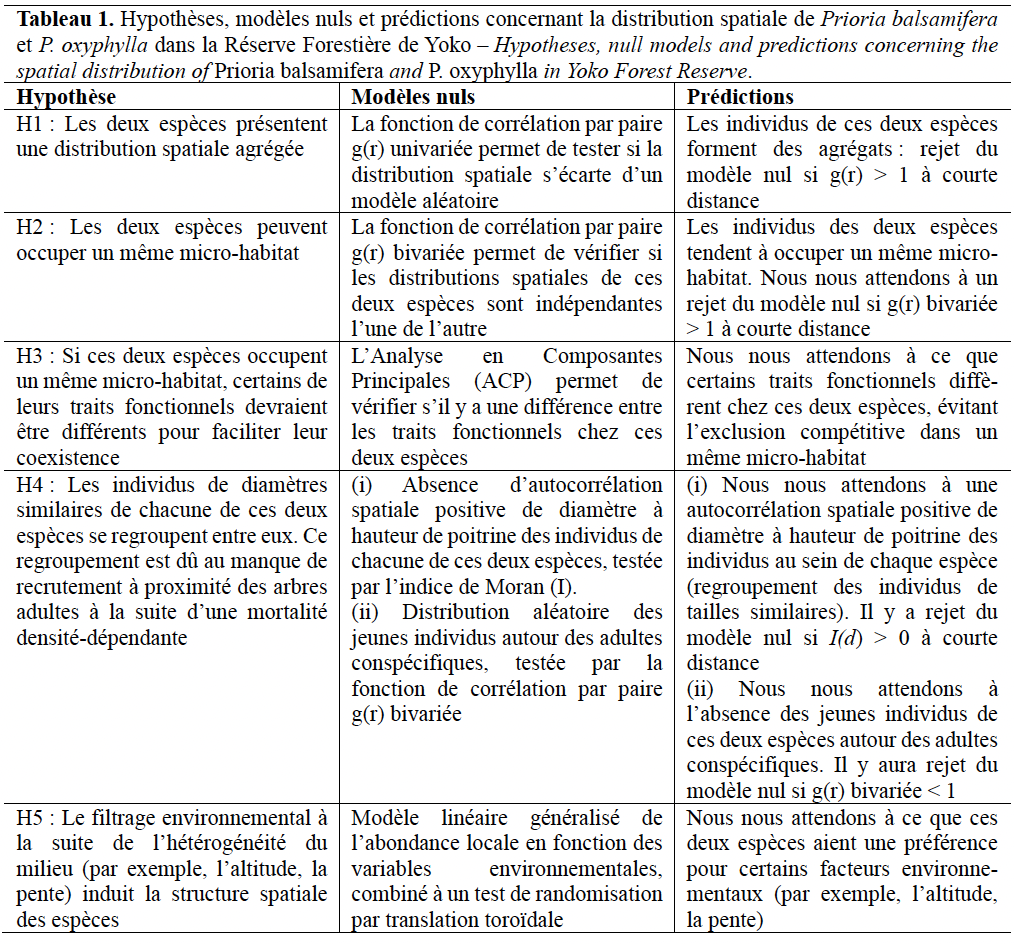
9Cette recherche sur la structure spatiale de P. balsamifera et P. oxyphylla aborde les questions suivantes dont les hypothèses, les modèles nuls et les prédictions sont précisés dans le tableau 1 :
10– quel est le modèle de la structure spatiale de ces espèces dans la Réserve Forestière de Yoko en RDC ?
11– ces deux espèces tendent-elles à occuper un même micro-habitat ?
12– si ces deux espèces occupent un même micro-habitat, leur coexistence peut-elle être expliquée par une complémentarité de leurs niches écologiques ?
13– quels sont les rôles de la taille des individus sur la structure spatiale de ces espèces dans ce milieu ?
14– quelles variables environnementales hétérogènes peuvent expliquer la structure spatiale de ces espèces dans la Réserve Forestière de Yoko ?
15Les résultats de cette étude sont nécessaires pour améliorer la connaissance sur l’écologie de ces deux espèces.
2. MATÉRIEL ET MÉTHODES
2.1. Description des espèces
16Prioria balsamifera et P. oxyphylla sont deux espèces du genre Prioria, appartenant à la sous-famille des Detarioideae, famille des Fabaceae (LPWG, 2017). Elles sont commercialisées respectivement sous le nom de tola (Tailfer, 1989 ; Cobbinah & Obeng, 2011 ; Meunier et al., 2015) ou d’agba, et de tchitola (Tailfer, 1989 ; Lemmens, 2011 ; Meunier et al., 2015). Ces deux espèces présentent des distributions géographiques très similaires en Afrique centrale : du sud du Nigéria jusqu’en RDC et vers le sud jusqu’à l’enclave de Cabinda en Angola (Cobbinah & Obeng, 2011 ; Lemmens, 2011 ; Bbidjo et al., 2024). Elles sont rencontrées dans les forêts semi-décidues et dans les forêts sempervirentes (Breteler, 1999 ; Cobbinah & Obeng, 2011 ; Lemmens, 2011 ; Meunier et al., 2015). Prioria balsamifera et P. oxyphylla ont des gousses ailées samaroïdes indéhiscentes. Ce sont des espèces anémochores (Sepulchre et al., 2008 ; Meunier et al., 2015) et semi-héliophiles (Bbidjo et al., 2024). Prioria balsamifera est placée sur la liste rouge de l’IUCN (2020) comme espèce en danger, ce qui n’est pas le cas de P. oxyphylla, considérée comme une espèce moins préoccupante, connaissant cependant une décroissance démographique et une baisse constante du nombre d’individus matures (Hills, 2019).
2.2. Milieu d’étude
17Cette étude a été réalisée dans la Réserve Forestière de Yoko au Nord-Est de la République Démocratique du Congo, dans la province de la Tshopo, à 32 km au Sud-Est de la ville de Kisangani, en territoire d’Ubundu sur la rive gauche du fleuve Congo, à 0°17’N et 25°18’E (Figure 1). L’altitude moyenne de la région est de 450 m (Vleminckx et al., 2015).
18Le climat est de type Af, selon la classification de Köppen (1936). Il est caractérisé par une température moyenne de 25 °C et des précipitations annuelles moyennes de 1 750 mm (Ndamiyehe et al., 2020). Le sol, considéré comme ferralsol, est acide (pH < 6) et fortement altéré (Van Wambeke et al., 1957 ; WRB, 2014). Ce sol a une forte teneur en sable avec dominance de quartz et une faible teneur en argile kaolinique et en oxyde de fer hydraté (WRB, 2014). La partie sud-ouest de la réserve est marquée par des sols bruns, sablo-argileux tandis que dans la partie nord-est, on retrouve des sols rouge ou rouge-jaune, argilo-sablonneux dans les horizons de surface et argilo-limono-sableux en profondeur (Lokonda, 2018).
19La Réserve Forestière de Yoko fait partie de la région phytogéographique Guinéo-Congolaise (White, 1983). Elle est couverte, dans sa partie nord, par des forêts sempervirentes monodominantes à Gilbertiodendron dewevrei (De Wild.) J.Léonard et, dans sa partie sud, par des forêts semi-caducifoliées et mixtes à Scorodophloeus zenkeri Harms (Lebrun & Gilbert, 1954 ; Evrard, 1968 ; Lomba & Ndjele, 1998). Parmi les espèces souvent rencontrées en sous-bois figurent celles du genre Diospyros, Cola bruneelii De Wild., Scaphopetalum thonneri De Wild. & T.Durand ou encore Microdesmis yafungana J.Léonard (Kahindo, 2011).
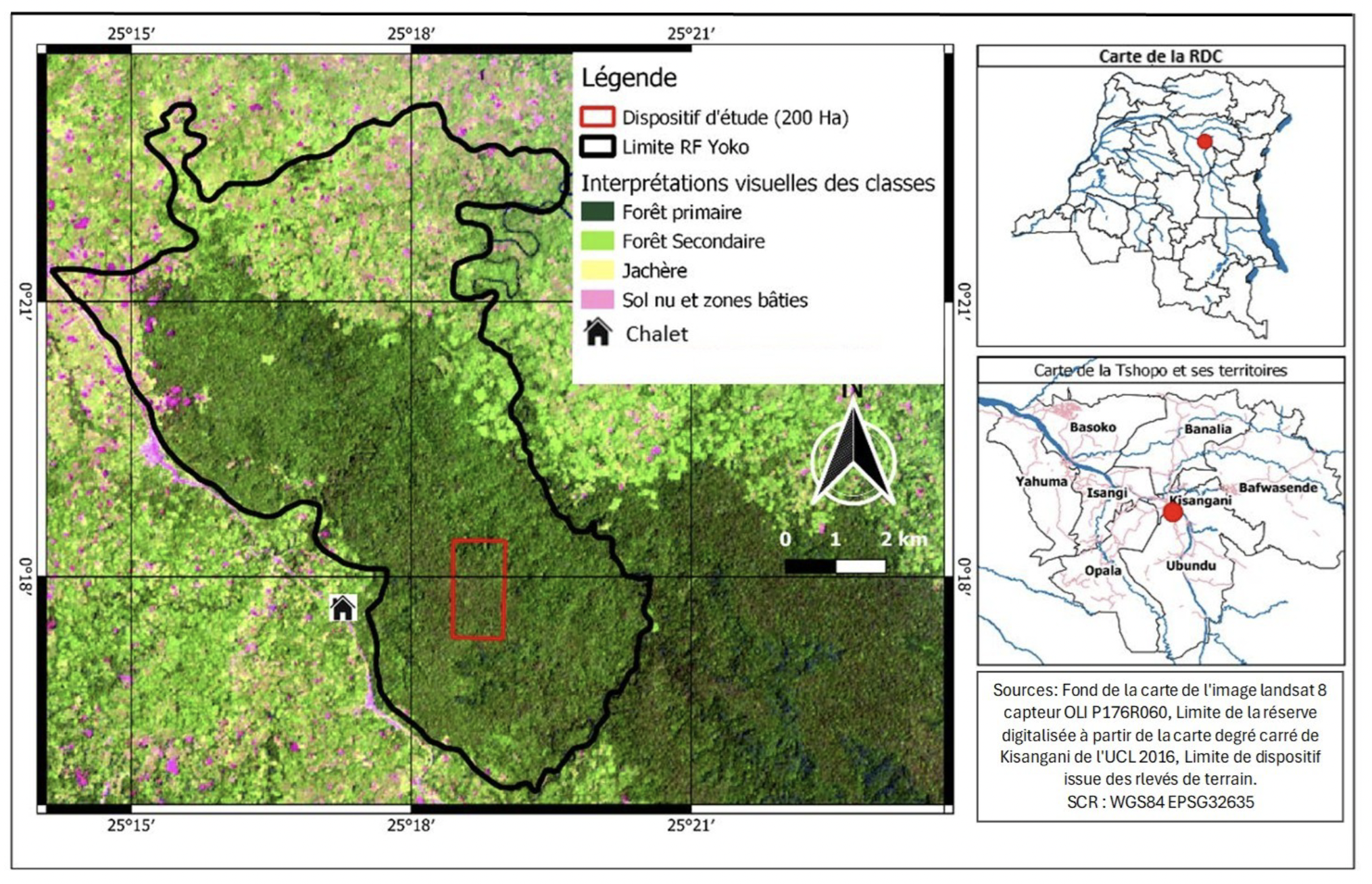
Figure 1. Carte de la localisation du milieu d’étude — Map of the location of the study area.
2.3. Protocole de collecte des données
20Les données ont été collectées dans une parcelle permanente de 200 ha, soit 2 000 m x 1 000 m, dans la forêt semi-caducifoliée de la Réserve Forestière de Yoko où tous les individus de P. balsamifera et P. oxyphylla à diamètre à hauteur de poitrine (dhp) ≥ 10 cm ont été répertoriés et cartographiés (Figure 2). L’inventaire a été réalisé dans des bandes de 50 m x 2 000 m, délimitées par des layons équidistants de 50 m, à l’aide d’une boussole et d’un décamètre permettant d’attribuer des coordonnées x,y à chaque arbre. Un numéro a été attribué, à l’aide d’une peinture, à chaque individu inventorié pour ne pas l’inventorier plus d’une fois.
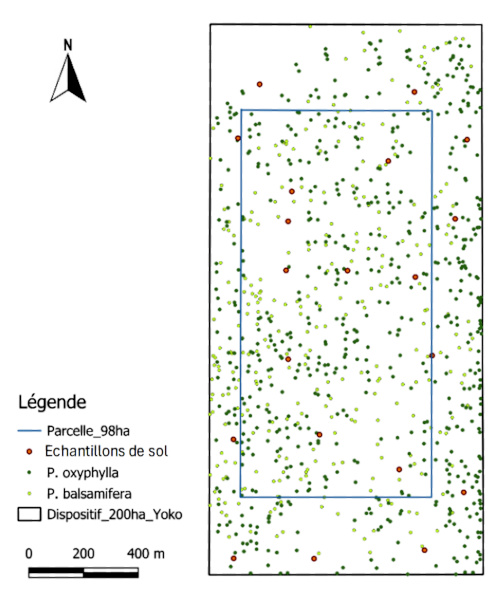
Figure 2. Position de Prioria balsamifera et P. oxyphylla et points d’échantillonnage des sols dans un dispositif de 200 ha – Position of Prioria balsamifera and P. oxyphylla and soil sampling points in a 200 ha plot.
21Pour déterminer les propriétés physiques du sol au sein de notre dispositif, la parcelle de 200 ha a été subdivisée en 200 placettes de 1 ha chacune. Les échantillons du sol ont été prélevés au centre de 20 placettes sélectionnées d’une façon aléatoire, réparties sur l’ensemble du dispositif. Étant donné que la proportion des différents éléments texturaux ne varie pas jusqu’au moins 100 cm de profondeur dans cette réserve tant au niveau du plateau qu’au niveau du bas-fonds (Lokonda et al., 2018), ces échantillons ont été prélevés à 50 cm de profondeur à l’aide d’une tarière. L’analyse granulométrique de ces échantillons a été réalisée par la méthode de sédimentation au laboratoire de pédologie de la Faculté de Gestion des Ressources Naturelles Renouvelables de l’Université de Kisangani.
22Pour avoir la position de chaque individu inventorié dans le dispositif de 200 ha par rapport à la pente et à l’altitude, les coordonnées cartésiennes de chaque arbre ont été transformées en coordonnées UTM. Les arbres ont été ensuite positionnés sur un raster de modèle numérique de terrain de 30 m de résolution, obtenu à partir d’une image satellitaire ASTER provenant de la NASA (www.earthdata.nasa.gov).
2.4. Analyses des données
23Caractérisation du modèle de distribution spatiale. La fonction de corrélation par paires (PCF) a été utilisée pour caractériser le modèle de distribution spatiale. Cette fonction détermine la configuration spatiale des arbres ainsi que les différentes échelles spatiales (Baddeley & Turner, 2005 ; Fibich et al., 2016). Elle est définie par la relation :
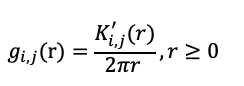
24où r est la distance entre les individus et K’i,j(r) est la dérivée de la fonction de Ripley Ki,j(r) (Ripley, 1987). La fonction de corrélation par paires (PCF) est univariée lorsqu’un seul type de point (i=j) est analysé. Elle est bivariée quand les analyses portent sur deux types de points différents (i≠j).
25La première hypothèse (H1) a été testée par la PCF univariée qui mesure le rapport entre la densité attendue de paires de points séparés par un rayon r et la densité moyenne de points sur toute la surface (Baddeley & Turner, 2005). La fonction indique si la distribution spatiale est aléatoire, agrégée ou régulière. Une distribution agrégée se caractérise par g(r) >1 pour r petit et g(r) qui tend à décroitre quand r augmente. Une distribution régulière se caractérise par g(r) <1 pour r petit et g(r) qui tend à croitre et tendre vers g(r)=1 quand r augmente.
26La PCF bivariée a permis de tester la deuxième hypothèse (H2). La fonction indique s’il y a une distribution indépendante (gij(r) = 1), une association positive (attraction ; gij(r) > 1) ou une association négative (répulsion ; gij(r) < 1) entre les individus de deux espèces de Prioria.
27La déviation du modèle observé par rapport à l’hypothèse nulle de distribution spatiale aléatoire (PCF univariée) ou indépendante (PCF bivariée) a été testée en comparant la fonction de distribution à l’intervalle de confiance généré par 100 simulations de Monte Carlo du modèle nul. Le package « spatstat » du logiciel R a été utilisé pour cette analyse (Luambua et al., 2021).
28Analyse de variation des traits fonctionnels chez ces deux espèces. Pour vérifier si certains traits fonctionnels diffèrent chez ces deux espèces (H3), nous avons réalisé une Analyse en Composantes Principales (ACP) en utilisant le package FactoMineR (version 2.11). Les 14 traits fonctionnels analysés, dont les données sont issues de la région de Yangambi et extraites de la base de données mondiale TRY (Kattge et al., 2020), sont : la surface foliaire spécifique (SFS, m2·kg-1), la teneur en carbone des feuilles par surface foliaire (CF/SF, mg·g-1), la teneur en carbone des feuilles par masse sèche des feuilles (CF/MS, g·m-2), la signature isotopique du carbone des feuilles (SICF, ‰), le rapport carbone/azote des feuilles (C/N, g·g-1), la teneur en matière sèche des feuilles (TMSF, g·g-1), la teneur en azote des feuilles par surface foliaire (NF/SF, g·m-2), la teneur en azote des feuilles par masse sèche des feuilles (NF/MSF, mg·g-1), la signature isotopique de l’azote foliaire (SINF, ‰), le rapport azote/phosphore des feuilles (N/P, g·g-1), la signature isotopique de l’oxygène des feuilles (SIOF, ‰), la teneur en phosphore des feuilles par surface foliaire (PF/SF, g·m-2), la teneur en phosphore des feuilles par masse sèche des feuilles (PF/MSF, mg·g-1) et la densité du bois (DB, g·cm-3). Pour faciliter la réalisation de l’ACP, les données manquantes chez certains traits (Tableau 2) ont été imputées par la méthode itérative grâce au package missMDA (version 1.20).

29Caractérisation de la distribution spatiale en fonction de la taille des individus. Pour tester la quatrième hypothèse (H4), l’indice I de Moran a été utilisé pour caractériser l’autocorrélation spatiale de diamètre à hauteur de poitrine des individus chez chaque espèce. Cet indice évalue le degré de similarité de diamètre à hauteur de poitrine entre les individus séparés par un intervalle de distance donné, d (Luambua et al., 2021). I(d) > 1 indique que les individus séparés par un intervalle de distance d sont spatialement autocorrélés. Cela veut dire qu’ils ont des diamètres à hauteur de poitrine plus similaires que les diamètres à hauteur de poitrine de deux individus pris au hasard, alors que les valeurs négatives indiquent la tendance inverse. Une valeur nulle suggère l’absence d’autocorrélation spatiale, c’est-à-dire une variation aléatoire du diamètre à hauteur de poitrine à l’échelle locale (de Frutos et al., 2007). Les résultats sont présentés sous forme d’un autocorrélogramme représentant les valeurs de I(d) en fonction d’intervalles de distance croissants. L’indice I de Moran est calculé par la formule :
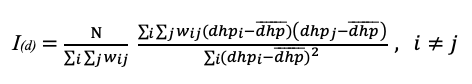
où N est le nombre total d’arbres, dhpi et dhpj sont les dhp respectifs des arbres i et j, wij = 1 si la distance géographique entre i et j est comprise dans l’intervalle de distance d, sinon wij = 0 et 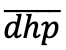 est le dhp moyen de tous les arbres. Les intervalles de distance ont été définis comme des plages qui ne se chevauchent pas et dont les distances maximales sont inférieures à 100, 200, 300 m, etc.
est le dhp moyen de tous les arbres. Les intervalles de distance ont été définis comme des plages qui ne se chevauchent pas et dont les distances maximales sont inférieures à 100, 200, 300 m, etc.
30L’indice d’autocorrélation spatiale I de Moran a permis de vérifier si des cohortes d’individus avec des diamètres à hauteur de poitrine similaires se regroupent dans l’espace. Le test de Mantel a été utilisé pour vérifier la signification de l’indice de Moran calculé (Potts et al., 2012 ; Luambua et al., 2021).
31Afin de vérifier si le regroupement des individus avec des diamètres à hauteur de poitrine similaires est dû au manque de recrutement à proximité des arbres adultes à la suite d’une mortalité dépendante de la distance aux arbres parents, la fonction de corrélation par paires g(r) bivariée a été utilisée. Cette fonction a permis d’analyser la relation spatiale entre les jeunes individus (10 cm ≤ dhp ˂ 30 cm) et les adultes (individus à dhp ≥ à 30 cm).
32Analyse de l’effet des facteurs environnementaux sur la distribution spatiale. Pour tester la quatrième hypothèse (H4), un modèle linéaire généralisé (GLM) avec une distribution de Poisson a été utilisé afin d’examiner dans quelle mesure les variables caractérisant l’hétérogénéité de l’habitat expliquent la distribution spatiale de ces deux espèces dans la Réserve Forestière de Yoko. La variable réponse étant l’abondance de chaque espèce de Prioria dans chacune des parcelles de 1 ha au sein du dispositif de 200 ha, les variables environnementales prises en compte dans cette étude étaient l’altitude et la pente. La significativité des coefficients de régression obtenus par le GLM a été évaluée par un test de randomisation par translation toroïdale (Harms et al., 2001), consistant à calculer la distribution des coefficients de régression pour 10 000 translations toroïdales aléatoires. La probabilité associée à un coefficient de régression est la proportion des coefficients de régression obtenus par translation toroïdale qui sont plus larges ou égaux en valeur absolue au coefficient observé.
33Toutes les analyses statistiques ont été réalisées avec le logiciel R version 4.4.1 (R Core Team, 2024).
34Analyses d’agrégation spatiale en excluant les zones de basse altitude. Ayant constaté que les espèces de Prioria évitent les zones de basse altitude sur notre dispositif, nous avons refait les analyses précédentes (agrégation spatiale et effet des facteurs environnementaux) au sein d’une parcelle rectangulaire de 98 ha centrée sur le plateau central (Figure 2) afin de vérifier la robustesse des résultats si les zones de basse altitude sont exclues.
3. RÉSULTATS
3.1. Structure diamétrique de P. balsamifera et P. oxyphylla
35Prioria balsamifera et P. oxyphylla présentent respectivement une densité de 2,72 individus·ha-1 et 5,48 individus·ha-1. L’analyse de la courbe de la structure diamétrique montre une distribution diamétrique en forme de J inversé chez ces deux espèces (Figure 3).
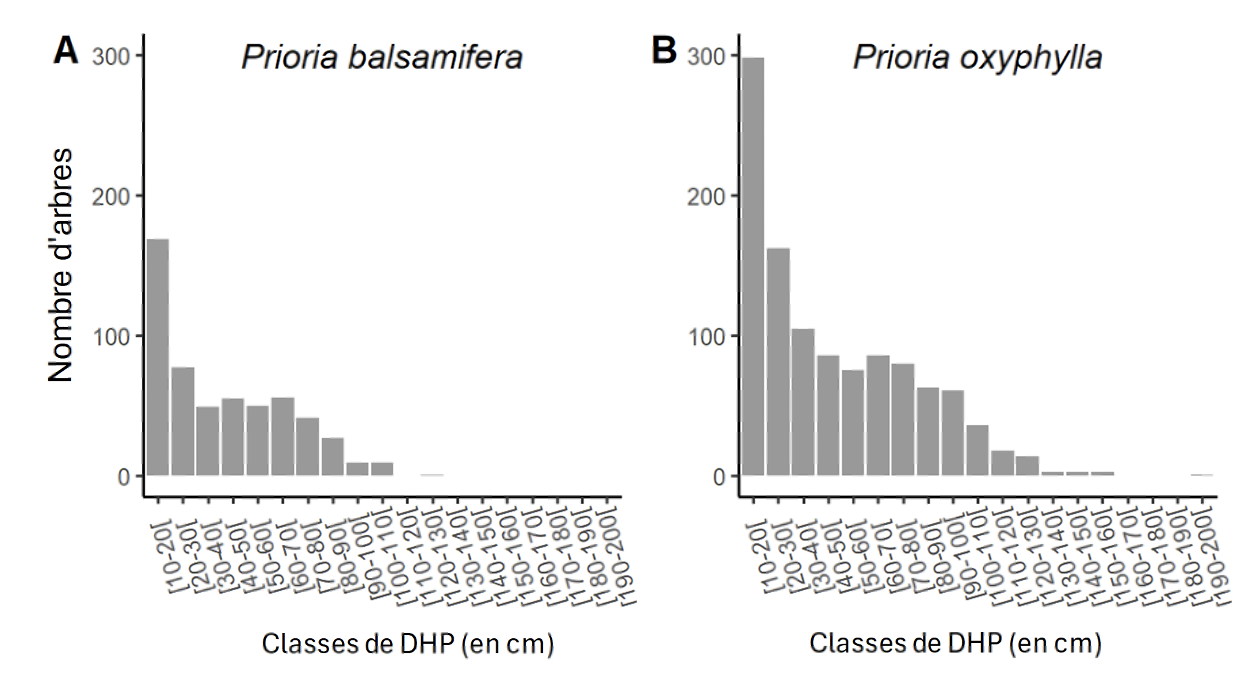
Figure 3. Structure diamétrique de Prioria balsamifera (A) et de P. oxyphylla (B) dans la Réserve Forestière de Yoko – Diameter structure of Prioria balsamifera (A) and P. oxyphylla (B) in the Yoko Forest Reserve.
3.2. Agrégation et occupation d’un même micro-habitat (Hypothèses 1 et 2)
36Prioria balsamifera et P. oxyphylla montrent chacune une distribution spatiale agrégée (g > 1 et au-dessus de l’intervalle de confiance) jusqu’à un rayon d’environ 850 m et 250 m, respectivement (Figure 4A et B). Par ailleurs, une attraction est observée entre les individus de P. balsamifera et P. oxyphylla dans un rayon d’environ 300 m (Figure 4C). Ces résultats soutiennent les deux premières hypothèses de cette étude qui suggèrent une distribution spatiale agrégée et une occupation d’un même micro-habitat par ces deux espèces dans la réserve forestière de Yoko.
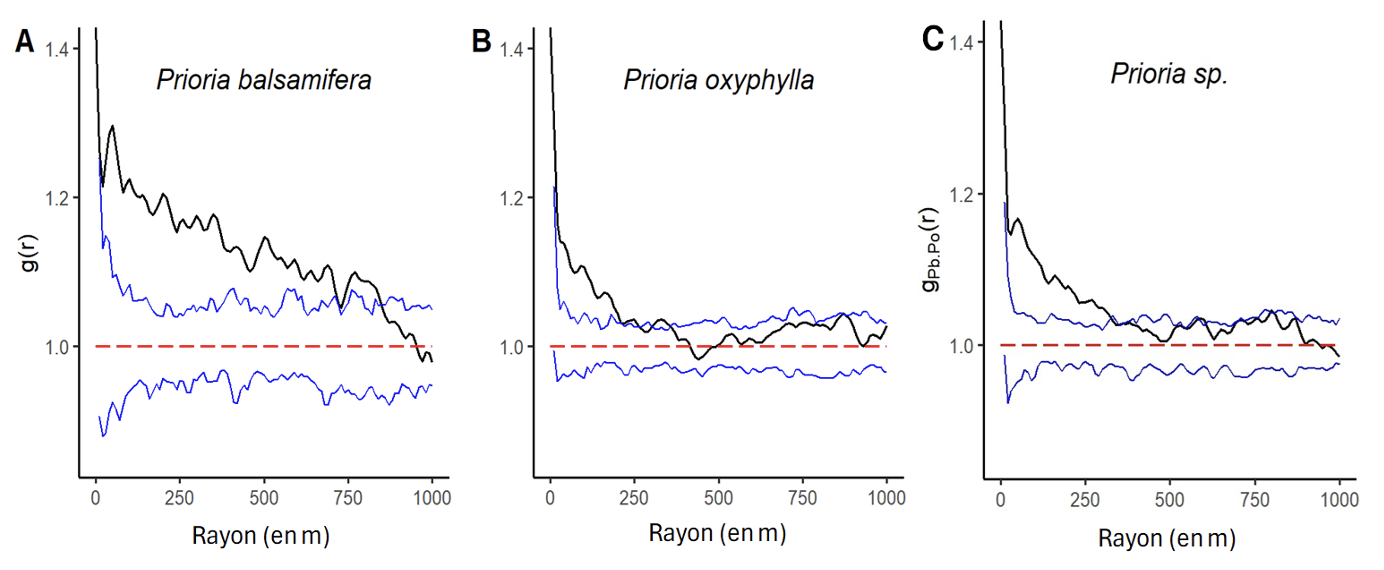
Figure 4. Fonction de corrélation de paires g(r) univariée (A) et (B), et bivariée (C) des individus de Prioria balsamifera et P. oxyphylla – Univariate (A) and (B), and bivariate (C) pairwise correlation function g(r) of Prioria balsamifera and P. oxyphylla individuals.
La ligne noire indique les valeurs observées ; les lignes bleues représentent l’intervalle de confiance au seuil de 0,05 sous l’hypothèse nulle ; les pointillés en rouge représentent les valeurs théoriques sous l’hypothèse nulle – The black line indicates the observed values; the blue lines represent the confidence interval at the 0.05 threshold under the null hypothesis; the red dots represent the theoretical values under the null hypothesis.
3.3. Variation des traits fonctionnels chez ces deux espèces (Hypothèse 3)
37L’analyse en composantes principales révèle une différenciation de certains traits fonctionnels entre ces deux espèces, soutenant notre hypothèse 3. La première dimension, qui est la plus discriminante, montre que P. balsamifera est corrélée à la surface foliaire spécifique (SFS), à la teneur en phosphore par masse sèche des feuilles (PF/MSF) et à la signature isotopique de carbone des feuilles (SICF) alors que P. oxyphylla est associée au rapport carbone/azote des feuilles (C/N) et à la teneur en carbone des feuilles
38par masse sèche des feuilles (CF/MS) (Figure 5).
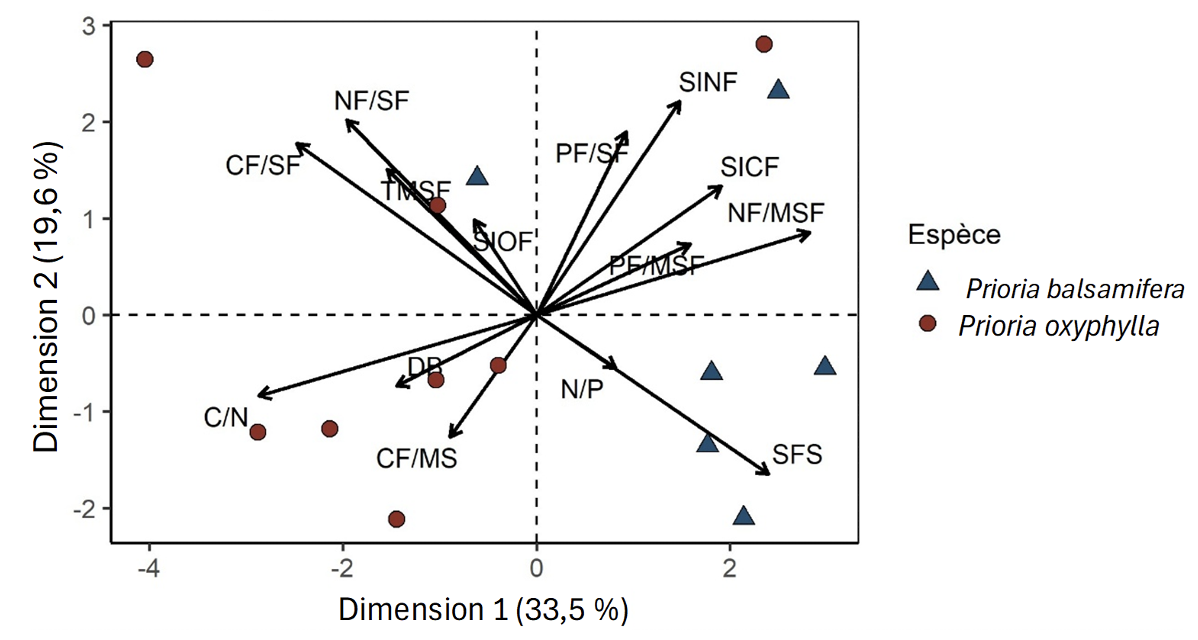
Figure 5. Analyse en Composantes Principales (ACP) de quelques traits fonctionnels de P. balsamifera et P. oxyphylla – Principal component analysis (PCA) of some functional traits of P. balsamifera and P. oxyphylla.
3.4. Regroupement des individus avec des diamètres à hauteur de poitrine similaires de chacune de ces deux espèces (Hypothèse 4)
39L’indice I de Moran montre une autocorrélation spatiale significativement positive des diamètres à hauteur de poitrine chez P. balsamifera, jusqu’à 150 m (Figure 6). Une tendance similaire est observée chez P. oxyphylla mais le signal est moins souvent significatif. Cette situation indique une tendance au regroupement spatial des arbres ayant des diamètres à hauteur de poitrine semblables. En outre, chez P. balsamifera, la structure spatiale des jeunes individus par rapport à la position des adultes est agrégée dans un rayon d’environ 500 m, alors que chez P. oxyphylla, cette tendance est à la limite du seuil de signification (Figure 7). On n’observe donc pas de distanciation des juvéniles par rapport aux adultes, contrairement à l’attendu de notre hypothèse 4.
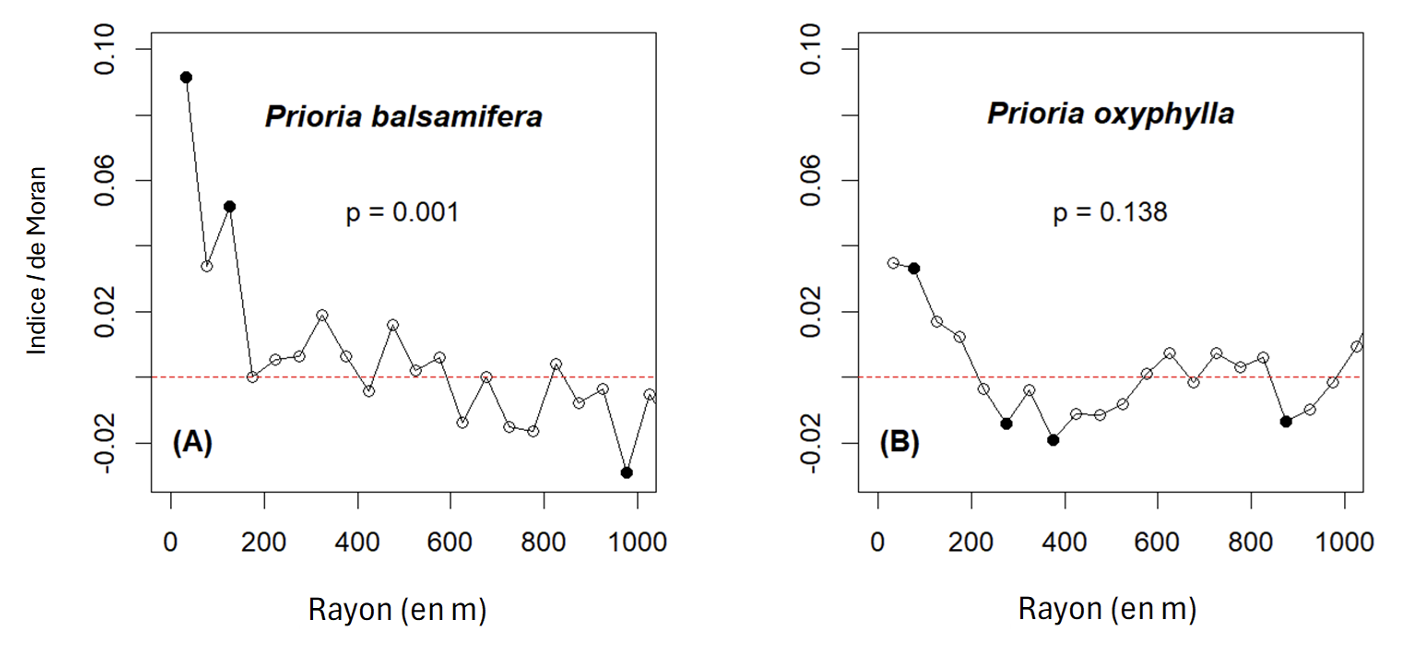
Figure 6. Indice I de Moran pour le diamètre à hauteur de poitrine de Prioria balsamifera (A) et P. oxyphylla (B) — Moran's I index for diameter at breast height of Prioria balsamifera (A) and P. oxyphylla (B).
Les points remplis en noir représentent les valeurs s’écartant significativement de l’intervalle de confiance à 95 %, contrairement aux points non remplis. La p-valeur rapporte la probabilité associée au test de Mantel – Filled dots in black represent values that deviate significantly from the 95% confidence interval, in contrast to unfilled dots. The p-value refers to the probability associated with the Mantel test.
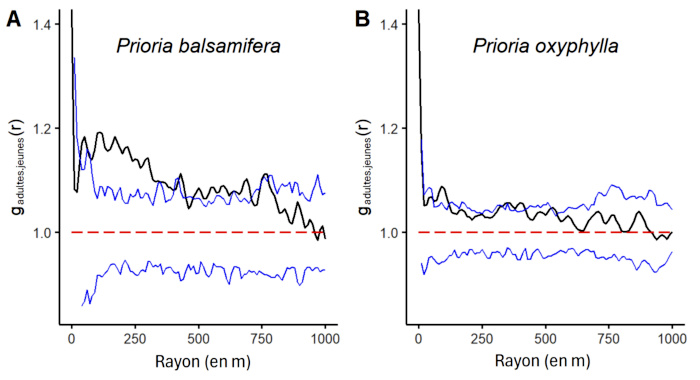
Figure 7. Fonction de corrélation de paires g(r) bivariée des jeunes individus (dhp < 30 cm) et adultes (dhp ≥ 30 cm) de Prioria balsamifera (A) et P. oxyphylla (B). La ligne noire indique les valeurs observées de la distribution des individus dans la surface d’étude ; les lignes bleues représentent l’intervalle de confiance au seuil de 0,05 et les traits en rouge représentent les valeurs théoriques sous l’hypothèse nulle – Bivariate pairwise correlation function g(r) of young (dbh < 30 cm) and adult (dbh ≥ 30 cm) individuals of Prioria balsamifera (A) and P. oxyphylla (B). The black line indicates the observed values of the distribution of individuals in the study area; the blue lines represent the confidence interval at the 0.05 threshold, and the red stippled lines represent the theoretical values under the null hypothesis.
3.5. Préférence pour certains facteurs environnementaux (Hypothèse 5)
40La texture du sol n’a pas été prise en considération dans la suite des analyses parmi les facteurs environnementaux pouvant influencer la distribution spatiale de P. balsamifera et P. oxyphylla dans notre dispositif d’étude, étant donné que les échantillons de sols étaient très homogènes avec 76,96 ± 2,83 % de sable, 16,84 ± 2,37 % d’argile et 6,2 ± 1,65 % de limon (Annexe 1).
41Concernant la pente et l’altitude, les individus de P. balsamifera et P. oxyphylla sont principalement dans les zones à pente ≤ 10 %, correspondant aux plateaux, et peu nombreux à l’extrême nord de la parcelle où on retrouve une série de bas-fond (Annexe 2). Par ailleurs, plus de la moitié des individus de ces deux espèces se retrouvent dans la zone où l’altitude est d’au moins 470 m (Figure 8).
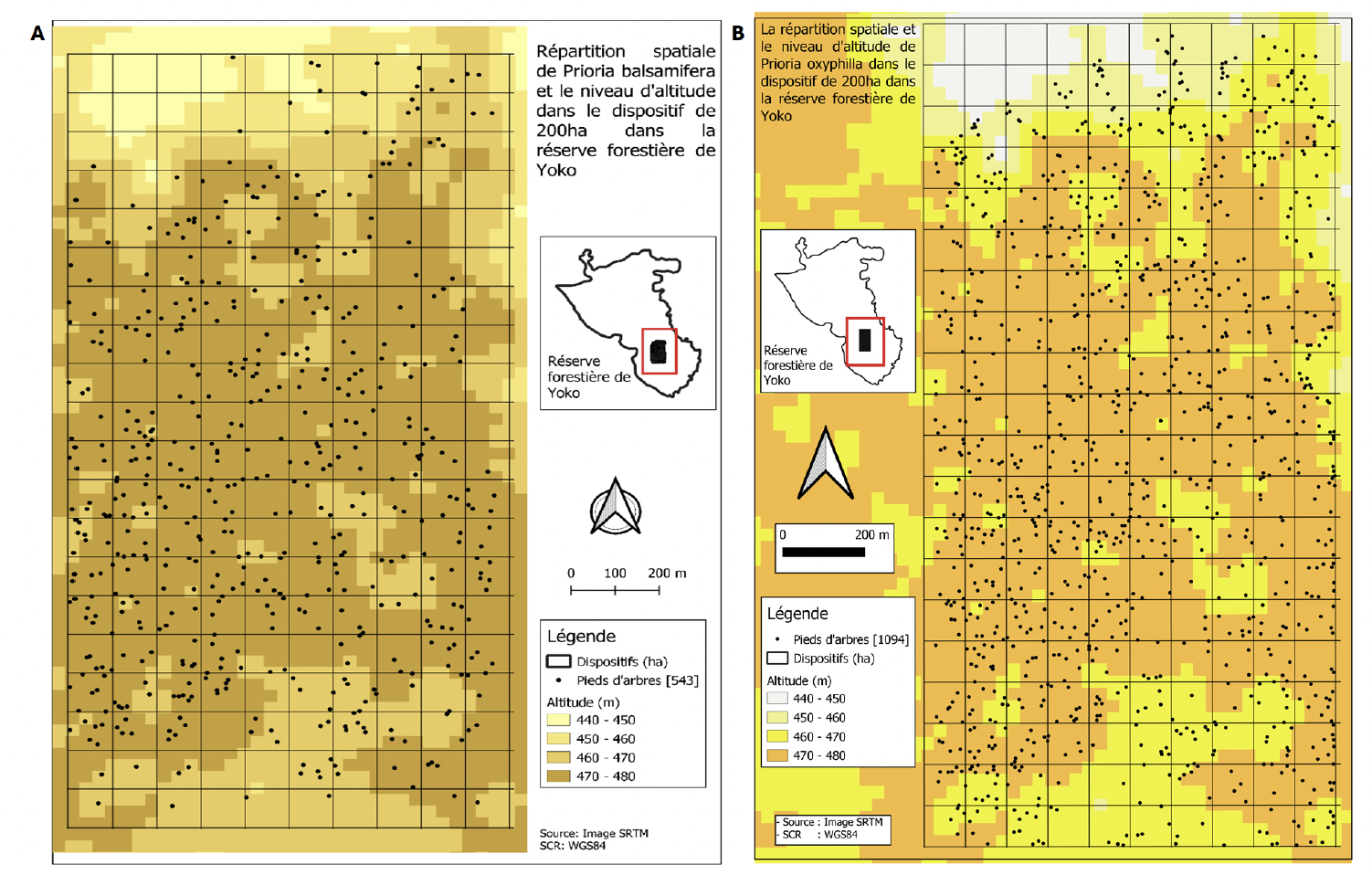
Figure 8. Localisation des individus de Prioria balsamifera (A) et de P. oxyphylla (B) à DHP ≥ 10 cm dans la parcelle de 200 ha sur un fond topographique (altitudes) – Location of Prioria balsamifera (A) and P. oxyphylla (B) individuals at DBH ≥ 10 cm in the 200 ha plot on a topographic background (altitudes).
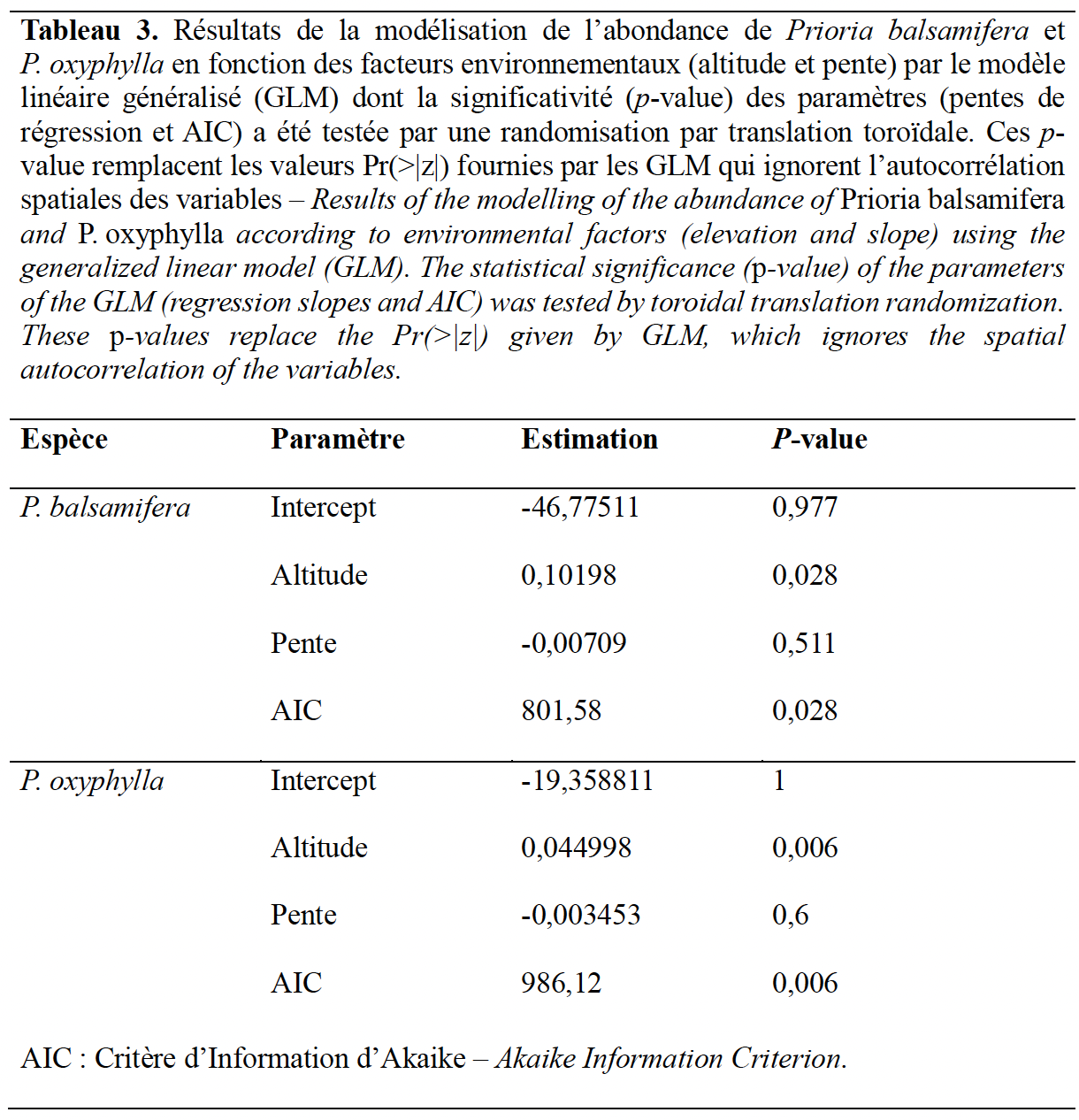
42Le modèle de régression indique que l’abondance des individus de P. balsamifera et P. oxyphylla est liée à l’altitude (Figure 9) et non à la pente. Le test de randomisation par translation toroïdale montre que ce lien est significatif tant chez P. balsamifera (p-value = 0,028) que chez P. oxyphylla (p-value = 0,006) (Tableau 3), soutenant l’hypothèse 5.
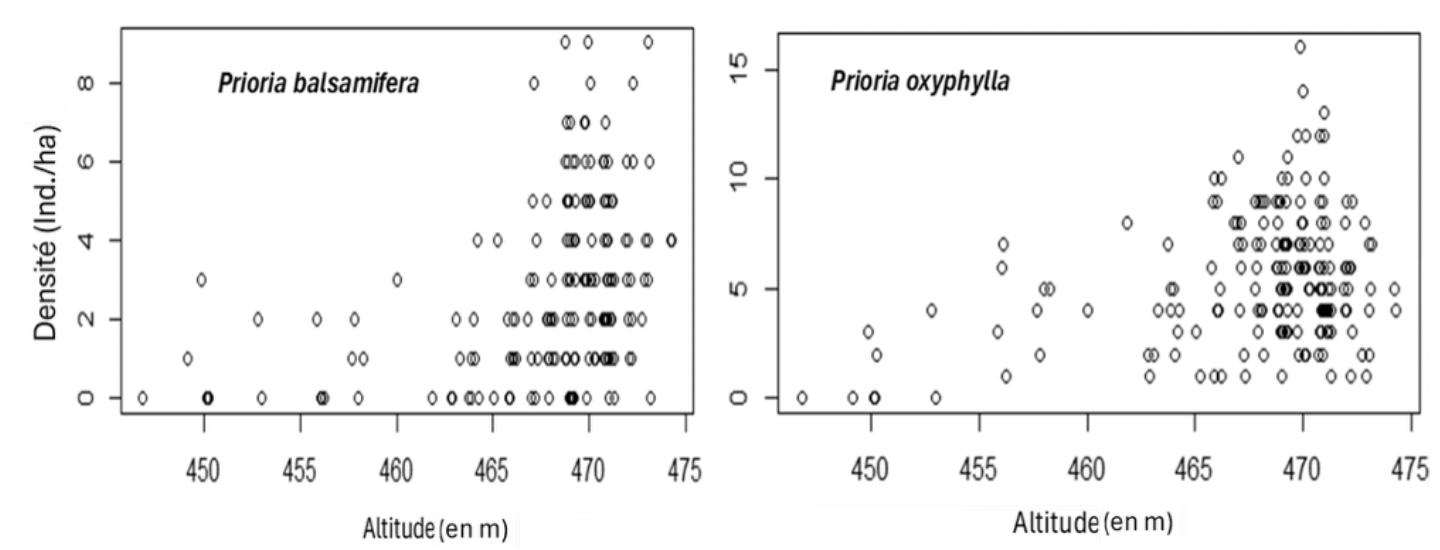
Figure 9. Lien entre la densité de Prioria balsamifera (gauche) et P. oxyphylla (droite) par parcelle de 1 ha et l’altitude – Relationship between the density of Prioria balsamifera (left) and P. oxyphylla (right) per 1 ha plot and elevation.
3.6. Robustesse des résultats en excluant les zones de basse altitude
43Lorsque les zones de basse altitude sont exclues, les patrons d’agrégation intra-espèces et inter-espèces sont nettement moins marqués et à la limite du seuil de significativité (Annexe 3), l’altitude n’explique plus significativement la densité des espèces (Annexe 4) et les juvéniles ne sont plus agrégés par rapport aux adultes (Annexe 5).
4. DISCUSSION
4.1. Prioria balsamifera et P. oxyphylla, espèces à structure agrégée dans la Réserve Forestière de Yoko
44Les deux espèces étudiées présentent une structure spatiale agrégée dans la parcelle de 200 ha (Figure 4A et 4B). La structure agrégée est le modèle de distribution spatiale le plus répandu chez les espèces d’arbres dans les forêts tropicales (Condit et al., 2000 ; Chao et al., 2007 ; Li et al., 2009 ; Kumba et al., 2013). Ces forêts sont caractérisées par une prépondérance d’espèces d’arbres de la famille des Fabaceae dont certaines espèces sont marquées par une faible dispersion de leurs diaspores (Van Der Burgt, 1997 ; Nebel et al., 2001 ; Jayakumar et al., 2009). La dispersion à faible distance occasionne une accumulation des graines non loin de leurs parents, ce qui renforce l’agrégation des individus (Nathan & Muller-Landau, 2000). Prioria balsamifera et P. oxyphylla ayant comme fruits des gousses ailées à une seule graine (samaroïdes) dispersées jusqu’à une distance moyenne de 50 m du semencier (Shaumba, 2009 ; Kidikwadi et al., 2015), il n’est pas exclu que leur agrégation soit liée à une faible dispersion de leurs diaspores. Cependant, cette agrégation est beaucoup moins marquée à l’échelle du plateau central où plus aucun effet de facteurs environnementaux pris en compte dans cette étude n’est observé (Annexe 3A et 3B). Ceci suggère que l’agrégation de ces deux espèces dans la Réserve Forestière de Yoko est principalement le résultat de l’évitement des bas-fonds. Toutefois, au regard de l’annexe 3, cette agrégation serait aussi liée à des effets de recrutement spatialement localisé à la suite des perturbations locales ou encore à des facteurs environnementaux non mesurés dans notre étude.
4.2. Prioria balsamifera et P. oxyphylla partagent un même micro-habitat
45Les résultats des analyses de relation spatiale entre les individus de P. balsamifera et P. oxyphylla montrent qu’il y a une répartition spatiale dépendante entre ces deux espèces dans la Réserve Forestière de Yoko (Figure 4C). En observant la figure 4, les agrégations intraspécifiques et interspécifiques sont assez semblables, ce qui confirme l’hypothèse de l’occupation d’un même micro-habitat par ces deux espèces de Prioria. Cependant, elles ne sont plus agrégées entre elles (Annexe 3C) lorsqu’on limite les analyses à une zone de 98 ha sur le plateau, échelle où il n’y a plus aucun effet des facteurs environnementaux (altitude et pente) sur l’abondance des deux espèces (Annexe 4). Ces résultats suggèrent que la dépendance de ces deux espèces dans la Réserve Forestière de Yoko résulte des préférences partagées pour le plateau. Nous n’avons toutefois pas pu identifier d’autres caractéristiques de ce micro-habitat. La texture du sol est apparue très homogène mais on ne peut exclure que d’autres propriétés du sol (fertilité, etc.) puissent favoriser chacune des deux espèces. Un recrutement corrélé des deux espèces à la suite de perturbations locales pourrait également expliquer leur agrégation.
4.3. Prioria balsamifera et P. oxyphylla ont des stratégies d’exploitation des ressources différenciées
46La différence de certains traits fonctionnels entre les deux espèces de Prioria (Figure 5) peut aussi faciliter le partage d’un même micro-habitat, en réduisant la compétition entre espèces (Pfenning et al., 2006 ; Long et al., 2011). Par sa surface foliaire spécifique et sa teneur en phosphore foliaire élevées, P. balsamifera semble avoir une stratégie d’exploitation des ressources plus acquisitive que P. oxyphylla, qui présente les traits d’une stratégie conservative. Ceci suggère que P. balsamifera favoriserait une croissance rapide aux dépens de la résistance aux stress.
4.4. Un recrutement autour des couronnes des adultes pourrait justifier l’autocorrélation spatiale positive de diamètres chez P. balsamifera et P. oxyphylla
47Les résultats d’autocorrélation spatiale des diamètres montrent que pour chacune de ces deux espèces, les arbres proches tendent à avoir des diamètres similaires. Ces résultats pouvaient soutenir l’hypothèse que les juvéniles s’installent loin des adultes suite à une mortalité densité dépendante. Toutefois, les analyses de la structure spatiale des jeunes individus par rapport aux individus adultes montrent que, chez P. balsamifera, les jeunes individus sont agrégés jusqu’à environ 500 m autour des adultes, sauf à très courte distance, probablement parce que les jeunes ne peuvent pas se maintenir sous la couronne d’un adulte. Chez P. oxyphylla, on observe des tendances similaires mais généralement non significatives. À l’échelle de la parcelle de 98 ha au niveau du plateau, les jeunes individus de P. balsamifera sont répartis indépendamment des adultes conspécifiques (Annexe 5), suggérant que l’agrégation des jeunes individus autour des adultes conspécifiques à l’échelle des 200 ha résulterait de l’évitement des bas-fonds. La situation est presque la même chez P. oxyphylla mais avec une agrégation des jeunes autour des adultes à une distance de 200 à 400 m (Annexe 5). Ces résultats montrent que les jeunes individus s’installent dans des zones où les facteurs environnementaux leur sont favorables, tout comme aux adultes, et que leur recrutement ne semble pas affecté par la présence d’adultes à proximité, à part probablement juste sous leurs couronnes.
48Une explication alternative à l’autocorrélation spatiale des diamètres des troncs, positive jusqu’à environ 100-150 m, pourrait être que le recrutement tende à se réaliser sur des aires limitées, changeantes au cours du temps, par exemple suite à des perturbations ouvrant la canopée, pour autant que la corrélation âge-diamètre soit étroite. On ne peut toutefois pas exclure que les vitesses de croissance varient selon les conditions environnementales locales et engendrent aussi une autocorrélation spatiale des diamètres.
4.5. L’abondance de P. balsamifera et P. oxyphylla est liée à l’altitude
49Nos résultats montrent que l’abondance des individus de P. balsamifera et P. oxyphylla est significativement liée à l’altitude dans la Réserve Forestière de Yoko. Plusieurs recherches réalisées en forêts tropicales ont reconnu les rôles non négligeables des facteurs édaphiques et topographiques dans la structuration spatiale de certaines espèces d’arbres (Gartlan et al., 1986 ; Collinet, 1997 ; Condit et al., 2000 ; Peh et al., 2011 ; Vleminckx et al., 2015 ; Luambua et al., 2021). Les espèces végétales peuvent présenter des performances de croissances diverses selon les habitats et ne peuvent survivre que là où les conditions le leur permettent (Ackerly, 2003). L’affinité de P. balsamifera et P. oxyphylla avec l’altitude dans la Réserve Forestière de Yoko peut être liée à leurs exigences face à certaines propriétés édaphiques.
50Dans cette étude, les analyses des propriétés édaphiques ont été limitées aux analyses granulométriques des sols prélevés dans quelques parcelles réparties sur l’ensemble de notre dispositif d’étude. Les résultats de ces analyses n’ont pas été pris en compte dans les analyses des effets des facteurs environnementaux sur la structure spatiale de Prioria, étant donné que le sable présentait une proportion très élevée et assez homogène dans toutes les parcelles échantillonnées. Il serait intéressant à l’avenir de prendre en compte les propriétés chimiques et physiques du sol pour mieux comprendre leur rôle sur la structure spatiale des espèces de Prioria.
5. CONCLUSIONS
51Cette étude avait pour objectif de caractériser la structure spatiale de P. balsamifera et P. oxyphylla dans la Réserve Forestière de Yoko. Les résultats montrent que ces deux espèces présentent des agrégations intraspécifique et interspécifique semblables, et une autocorrélation de diamètre à hauteur de poitrine positive de leurs individus. Les jeunes individus de P. balsamifera s’installent autour des adultes conspécifiques mais au-delà de leurs couronnes, un effet moins marqué chez P. oxyphylla. Par ailleurs, cette étude montre que, dans un contexte d’hétérogénéité environnementale, l’agrégation chez ces deux espèces dans la Réserve Forestière de Yoko est largement due à l’évitement des bas-fonds et pourrait être facilitée par une certaine différenciation de niche écologique.
52Comme cette étude n’a pas pris en compte tous les facteurs pouvant expliquer la structure spatiale de ces deux espèces dans la Réserve Forestière de Yoko, des études intégrant d’autres propriétés physiques et les propriétés chimiques du sol ainsi qu’une quantification de la dispersion des diaspores de ces deux espèces sont nécessaires pour améliorer la compréhension des facteurs écologiques qui influencent leur structure spatiale.
Remerciements
53Les travaux de terrain ont été couverts par la subvention de CARN (Conservation Action Research Network) dont Vivien BBIDJO est bénéficiaire. La rédaction de cet article a été finalisée à l’ULB (Université Libre de Bruxelles) grâce à la bourse de doctorat octroyée à Vivien BBIDJO par ARES-ULB (Académie de Recherche et d’Enseignement Supérieur-Université Libre de Bruxelles).
54Conflits d’intérêts
55Les auteurs ne déclarent aucun conflit d’intérêts.
Bibliographie
Ackerly D., 2003. Community assembly, niche conservatism, and adaptive evolution in changing environments. Int. J. Plant Sci., 164, 165-184, doi.org/10.1086/368401
Altman J. et al., 2016. Linking spatiotemporal disturbance history with tree regeneration and diversity in an old-growth forest in northern Japan. Perspect. Plant Ecol. Evol. Syst., 21, 1-13, doi.org/10.1016/j.ppees.2016.04.003
Baddeley A. & Turner R., 2005. Spatstat: an R package for analyzing spatial point patterns. J. Stat. Software, 12, 1-42.
Bbidjo V. et al., 2024. Prioria balsamifera (Vermoesen) Breteler et Prioria oxyphylla (Harms) Breteler : traits d’histoire de vie et perspectives pour des recherches futures. Bois For. Trop., 359, 85-95, doi.org/10.19182/bft2024.359.a37087
Boulangeat I., Gravel D. & Thuiller W., 2012. Accounting for dispersal and biotic interactions to disentangle the drivers of species distributions and their abundances. Ecol. Lett., 15, 584-593, doi.org/10.1111/j.1461-0248.2012.01772.x
Breteler F.J., 1999. A revision of Prioria, including Gossweilerodendron, Kingiodendron, Oxystigma, and Pterygopodium (Leguminosae – Caesalpinioideae – Detarieae) with emphasis on Africa. Wageningen Agricultural University, The Netherlands: Herbarium Vadense, 99-3, https://library.wur.nl/WebQuery/wurpubs/fulltext/282989, (04/02/2026).
Brienen R.J.W. et al., 2015. Long-term decline of the Amazon carbon sink. Nature, 519, 344-348, doi.org/10.1038/nature14283
Chao W. et al., 2007. Distribution patterns of tree species in the Lanjenchi lowland rain forest. Taiwania, 52, 343-351, doi.org/10.6165/tai.2007.52(4).343
Cobbinah J.R. & Obeng E.A., 2011. Prioria balsamifera (Vermoesen) Breteler. In : Lemmens R.H.M.J., Louppe D. & Oteng Amoako A.A., eds. PROTA. Wageningen, The Netherlands: PROTA, https://plantuse.plantnet.org/en/Prioria_balsamifera_(PROTA), (04/02/2026).
Collinet F., 1997. Essai de regroupement des principales espèces structurantes d’après l’analyse de leur répartition spatiale (Forêt de Paracou-Guyane). Thèse de doctorat: Université Claude Bernard - Lyon 1 (France).
Condit R. et al., 2000. Spatial patterns in the distribution of tropical tree species. Science, 80(288), 1414-1418.
Condit R. et al., 2013. Species distributions in response to individual soil nutrients and seasonal drought across a community of tropical trees. PNAS, 110, 5064-5068, doi.org/10.1073/pnas.1218042110
Connell J.H., 1971. On the role of natural enemies in preventing competitive exclusion in some marine mammals and in rain forest trees. In: den Boer P.J. & Gradwell G.R., eds. Dynamics of populations. Wageningen, The Netherlands : Center for Agricultural Publishing and Documentation (PUDOC), 298-312.
De Araújo C.B., Marcondes-Machado L.O. & Costa G.C., 2014. The importance of biotic interactions in species distribution models: a test of the Eltonian noise hypothesis using parrots. J. Biogeogr., 41, 513-523, doi.org/10.1111/jbi.12234
de Frutos A., Olea P.P. & Vera R., 2007. Analyzing and modelling spatial distribution of summering lesser kestrel: the role of spatial autocorrelation. Ecol. Modell., 200, 33-44, doi.org/10.1016/j.ecolmodel.2006.07.007
Evrard C., 1968. Recherches écologiques sur le peuplement forestier des sols hydromorphes de la Cuvette centrale congolaise. Bruxelles : INEAC, série scientifique n°110.
Fibich P. et al., 2016. Spatial patterns of tree species distribution in New Guinea primary and secondary lowland rain forest. J. Veg. Sci., 27, 328-339, doi.org/10.1111/jvs.12363
Gartlan J.S., Newbery D.M.C., Thomas D.W. & Waterman P.G., 1986. The influence of topography and soil phosphorus on the vegetation of Korup forest reserve, Cameroun. Vegetatio, 65, 131-148, doi.org/10.1007/BF00044814
Gemerden B.S.V., Shu G.N. & Olff H., 2003. Recovery of conservation values in Central African rain forest after logging and shifting cultivation. Biodivers. Conserv., 12(8), 1553-1570, doi.org/10.1023/A:1023603813163
Grantham H.S. et al., 2020. Spatial priorities for conserving the most intact biodiverse forests within Central Africa. Environ. Res. Lett., 15, 1-13, doi.org/10.1088/1748-9326/ab9fae
Hardy O.J. & Sonké B., 2004. Spatial pattern analysis of tree species distribution in a tropical rain forest of Cameroon: assessing the role of limited dispersal and niche differentiation. For. Ecol. Manage., 197, 191-202, doi.org/10.1016/j.foreco.2004.05.014
Harms K.E., Condit R., Hubbel S.P. & Foster R., 2001. Habitat associations of trees and shrubs in a 50-ha neotropical forest plot. J. Ecol., 89, 947-959, doi.org/10.1111/j.1365-2745.2001.00615.x
Hills R., 2019. Prioria oxyphylla. The IUCN Red List of Threatened Species 2019: e.T62027002A62027008, doi.org/10.2305/IUCN.UK.20193.RLTS.T62027002A62027008.en
Howe H.F., 1989. Scatter-and clump-dispersal and seedling demography : hypothesis and implications. Oecologia, 79, 417-426.
Hubau W. et al., 2020. Asynchronous carbon sink saturation in African and Amazonian tropical forests. Nature, 579, 80-87, doi.org/10.1038/s41586-020-2035-0
IUCN (International Union for Conservation of Nature and Natural Resources), 2020. IUCN Red list of threatened species. Cambridge, UK: IUCN, www.iucnredlist.org, (14/09/2021).
Janzen D.H., 1970. Herbivores and the number of tree species in tropical forests. Am. Nat., 104, 501-528, https://www.jstor.org/stable/2459010, (04/02/2026).
Jayakumar S., Ramachandran A. & Heo J., 2009. Comparison of floristic diversity of evergreen forest inferred from different sampling approaches in the Eastern Ghats of Tamil Nadu, India. Curr. Sci., 96(4), 575-581, https://www.jstor.org/stable/24105473, (04/02/2026).
Kahindo M., 2011. Potentiel en produits forestiers autres que le bois d’œuvre dans les formations forestières de la région de Kisangani. Cas des rotins Eremospatha haullevilleana De Wild. et Laccosperma secundiflorum (P. Beauv.) Küntze de la Réserve Forestière de Yoko (Province Orientale, RD Congo). Thèse de doctorat : Faculté des Sciences, Université de Kisangani (RDC).
Kattge J. et al., 2020. TRY plant trait database – enhanced coverage and open access. Global Change Biol., 26, 119-188, doi.org/10.1111/gcb.14904
Kidikwadi T.E., Lubini A.C., Luyindula N. & Belesi K.H., 2015. Note préliminaire sur l’écologie et mesure de biomasse de Prioria balsamifera dans les stations forestières de l’INERA de Luki et Kiyaka en RD Congo. Int. J. Innovation Appl. Stud., 11(4), 914-927.
Köppen W., 1936. Das geographische system der klimate. In: Köppen W. & Geiger R., eds. Handbuch der klimatologie. Berlin: Verlag von Gebrüder Borntraeger.
Kumba S. et al., 2013. Structure spatiale des trois espèces les plus abondantes dans la Réserve Forestière de la Yoko, Ubundu, République Démocratique du Congo. Tropicultura, 31, 53-61, doi.org/10.4267/2042/5741
Lebrun J.-P. & Gilbert G., 1954. Une classification écologique des forêts du Congo. Bruxelles : INEAC, série scientifique n° 63.
Lemmens R.H.M.J., 2011. Prioria oxyphylla (Harms) Breteler. In: PROTA4U. Lemmens R. H. M. J., Louppe D., Oteng-Amoako A. A. (eds). https://www.prota4u.org/, (18/02/26).
Levi T. et al., 2019. Tropical forest can maintain hyperdiversity because of enemies. PNAS, 116, 581-586, doi.org/10.1073/pnas.1813211116
Li L. et al., 2009. Spatial distributions of tree species in a subtropical forest of China. Oikos, 118, 495-502, doi.org/10.1111/j.1600-0706.2009.16753.x
Lokonda M., 2018. Structure forestière, propriétés physico-chimiques du sol et indices pédoanthrocologiques de perturbations comparés entre la forêt monodominante à Gilbertiodendron dewevrei (De Wild.) J. Léonard et la forêt mixte adjacente. Thèse de doctorat : Faculté de Gestion des Ressources Naturelles Renouvelables, Université de Kisangani (RDC).
Lokonda M., Freycon V., Gourlet-Fleury S. & Kombele F., 2018. Are soils under monodominant Gilbertiodendron dewevrei and under adjacent mixed forests similar? A case study in the Democratic Republic of Congo. J. Trop. Ecol., 34(3), 176-185, doi.org/10.1017/S0266467418000135
Lomba B.L. & Ndjele M., 1998. Utilisation de la méthode de transect en vue de l’étude de la phytodiversité de Yoko (Ubundu-Congo). Ann. Fac. Sci. Unikis, 11, 35-46.
Long W., Zang R. & Schamp S.B., 2011. Within- and among-species variation in specific leaf area drive community assembly in a tropical cloud forest. Coecologia, 167, 1103-1113, doi.org/10.1007/s00442-011-2050-9
LPWG, 2017. A new subfamily classification of the Leguminiosae based on a taxonomically comprehensive phylogeny. Taxon, 66(1), 44-77, doi.org/10.12705/661.3
Luambua N.K. et al., 2021. Spatial patterns of light-demanding tree species in the Yangambi rainforest (Democratic Republic of Congo). Ecol. Evol., 11, 18691-18707, doi.org/10.1002/ece3.8443
Meunier Q., Moumbogou C. & Doucet J.-L., 2015. Les arbres utiles du Gabon. Gembloux, Belgique : Les Presses Agronomiques de Gembloux.
Morneau F., 2007. Effets d’un gradient d’engorgement sur la structure et la dynamique d’une forêt tropicale humide (Paracou, Guyane française). Thèse de doctorat : ENGREF, AgroParisTech (France).
Nathan R. & Muller-Landau H.C., 2000. Spatial patterns of seed dispersal, their determinants and consequences for recruitment. Tree, 15, 278-285.
Ndamiyehe J.B. et al., 2020. Quantifier les dimensions des houppiers à l’aide d’images aériennes à haute résolution pour estimer l’accroissement diamétrique des arbres dans les forêts d'Afrique centrale. Bois For. Trop., 343, 67-81, doi.org/10.19182/bft2020.343.a31848
Nebel G. et al., 2001. Structure and floristic composition of flood plain forests in the Peruvian Amazon: I. Overstorey. For. Ecol. Manage., 150, 25-57, doi.org/10.1016/S0378-1127(00)00680-0
Newbery D.McC., Gartlan J.S., McKey D.B. & Waterman P.G., 1986. The influence of drainage and soil phosphorus on the vegetation of Douala-Edea forest reserve, Cameroun. Vegetatio, 65(3), 149-162, https://link.springer.com/content/pdf/10.1007/BF00044815.pdf, (05/02/2026).
Peh K.S.-H. et al., 2011. Soil does not explain monodominance in a central African tropical forest. PLoS One, 6, 1-9, doi.org/10.1371/journal.pone.0016996
Pfennig D.W., Rice A.M. & Martin R.A., 2006. Ecological opportunity and phenotypic plasticity interact to promote character displacement and species coexistence. Ecology, 87, 769-779, doi.org/10.1890/05-0787
Potts M.D. et al., 2012. Habitat patterns in tropical rain forests: a comparison of 105 plots in Northwest Borneo. Ecology, 83, 2782-2797, doi.org/10.1890/0012-9658(2002)083[2782:HPITRF]2.0.CO;2
R Core Team, 2024. R: A language and environnement for statistical computing. Vienne : Fondation R pour l'informatique statistique, https://www.r-project.org
Réjou-Méchain M. et al., 2008. Regional variation in tropical forest tree species composition in the Central African Republic: an assessment based on inventories by forest companies. J. Trop. Ecol., 24, 663-674, doi.org/10.1017/S0266467408005506
Réjou-Méchain M. et al., 2011. Spatial aggregation of tropical trees at multiple spatial scales. J. Ecol., 99, 1373-1381, doi.org/10.1111/j.1365-2745.2011.01873.x
Ripley B.D., 1987. Spatial point pattern analysis in ecology. In: Legendre P. & Legendre L., eds. Developments in numerical ecology. Berlin; Heidelberg, Germany: Springer-Verlag, 407-429.
Sepulchre F., Dainou K. & Doucet J.-L., 2008. Étude de la vulnérabilité de 18 essences ligneuses commerciales d’Afrique centrale reprises sur la liste rouge IUCN. Gembloux, Belgique : Nature+, ATIBT, Gembloux Agro-Bio-Tech, https://www.atibt.org/files/upload/technical-publications/Etude_vulnerabilite__Gembloux_2008.pdf, (04/02/2026).
Shaumba K., 2009. Analyse de la régénération et de la répartition spatiale des Fabaceae-Caesalpionioideae dans la forêt de Yoko (Kisangani, R.D. Congo) : cas de Prioria balsamifera J.Leonard, Prioria oxyphylla (Vermoesen) Breteler et Scorodophloeus zenkeri Harms. Mémoire de DEA : Université de Kisangani (République Démocratique du Congo).
Sosef S.M.M. et al., 2021. Red list of the endemic and subendemic trees of central Africa (Democratic Republic of the Congo-Rwanda-Burundi). Meise, Belgium: Meise Botanic Garden, doi.org/10.5281/zenodo.5645166
Tailfer Y., 1989. La forêt dense d’Afrique centrale. Identification pratique des principaux arbres, tomes 1 et 2. Paris : CTA.
Terborgh J., 2020. At 50, Janzen-Connell has come of age. BioScience, 70(12), 1082-1092, doi.org/10.1093/biosci/biaa110
Van Der Burgt X.M., 1997. Explosive seed dispersal of the rainforest tree Tetraberlinia moreliana (Leguminosae-Caesalpinioideae) in Gabon. J. Trop. Ecol., 13(1), 145-151.
Van Wambeke A. et al., 1957. Notice explicative de la carte des sols et de la végétation du Congo belge et du Ruanda-Urundi. 6. Yangambi : planchette 3 : Lilanda, A et B. Bruxelles : INEAC.
Vleminckx J. et al., 2015. Impact of fine-scale edaphic heterogeneity on tree species assembly in a central African rainforest. J. Veg. Sci., 26, 134-144, doi.org/10.1111/jvs.12209
White F., 1983. The vegetation of Africa. A descriptive memoir to accompany the UNESCO/AETFAT/UNSO vegetation map of Africa. Paris: UNESCO.
WRB (World Reference Base), 2014. International soil classification system for naming soils and creating legends for soil maps. Roma : FAO.

